
アピキサバン
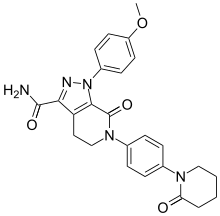
| |

| |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Eliquis |
| ライセンス | EMA:リンク |
| 法的規制 |
|
| 投与方法 | Oral |
| 薬物動態データ | |
| 生物学的利用能 | ~50% |
| 血漿タンパク結合 | ~87% |
| 代謝 | CYP3A4, CYP3A5, CYP1A2 and others |
| 半減期 | 9–14 h |
| 排泄 | Biliary (75%), renal (25%) |
| 識別 | |
|
CAS番号 |
503612-47-3 |
| ATCコード | B01AF02 (WHO) |
| PubChem | CID: 10182969 |
| IUPHAR/BPS | 6390 |
| DrugBank |
DB07828 |
| ChemSpider |
8358471 |
| UNII |
3Z9Y7UWC1J |
| KEGG |
D03213 |
| ChEMBL |
CHEMBL231779 |
| 化学的データ | |
| 化学式 | C25H25N5O4 |
| 分子量 | 459.497 g/mol |
| |
アピキサバン(Apixaban、開発コードBMS-562247-01)は、血栓塞栓症の治療・予防に用いられる、経口投与が可能な抗凝固剤の1つである。商品名エリキュース。血液凝固因子の1種であるXa因子を薬剤そのものが阻害する、直接Xa因子阻害薬に分類される。また、第Xa因子は酵素なので、酵素阻害剤に分類される薬剤でもある。なお、肝代謝型(肝排泄型)の薬剤としても知られる。
欧州で2012年4月に、日本で2012年12月に、米国で2012年12月に承認された。当初の承認は心房細動患者の血栓症予防であったが、2014年〜2015年に静脈血栓塞栓症の治療と再発予防について追加承認された。
効能・効果
日本で承認されている効能・効果は、
- 非弁膜症性心房細動患者における虚血性脳卒中および全身性塞栓症の発症抑制
- 静脈血栓塞栓症(深部静脈血栓症および肺血栓塞栓症)の治療および再発抑制
である。
英語版の添付文書に記載されている適応は、
- 非弁性心房細動患者の脳梗塞および塞栓症リスクの減少
- 膝関節置換術または股関節置換術を受けた患者の肺血栓塞栓症(PE)の原因となり得る深部静脈血栓症(DVT)予防
- DVTおよびPEの治療
- 治療後のDVTおよびPE再発防止
である。
心房細動
アピキサバンは英国国立医療技術評価機構から、以下の1つ以上に該当する非弁膜症性心房細動患者での脳梗塞および全身性塞栓症の予防薬として推奨されている。
アピキサバン、ダビガトラン、リバーロキサバン等の(新規)経口抗凝固薬は、心房細動の患者でワルファリンと同程度に非出血性脳梗塞を予防し、頭蓋内出血のリスクは低いとされる。
副作用
重大な副作用として規定されているものは、出血(頭蓋内出血(頻度不明)、消化管出血(0.6%)、眼内出血(0.3%)等)、間質性肺疾患、肝機能障害である。
充分に用いずに経口抗凝固薬の服用を早期中止すると、治療完遂後の血栓発生率や治療中の出血率よりも高い頻度で血栓を生じる。しかしこれは抗凝固薬を用いない状態での血栓出現率に戻っただけで、投与中止による反跳作用ではない。この危険性を低下させるためには他の抗凝固薬を用いるべきであるとされる。
出血
アピキサバンは出血の危険性を増大させ、重篤な、時に致死的な出血の原因となる。止血に影響を与える薬剤(他の抗凝固薬、ヘパリン、アスピリン、抗血小板薬、選択的セロトニン再取り込み阻害薬、セロトニン・ノルアドレナリン再取り込み阻害薬、非ステロイド性抗炎症薬)との併用は出血の危険性をさらに増大させる。
アピキサバンを用いる際の懸念事項として、薬物活性を中和する手段がない事が挙げられる。これは患者が緊急手術を受けられない事を意味し、ワルファリンと比べた際の大きな欠点と言える。
待機的手術又は侵襲的手技を実施する場合、休薬期間は低リスク手技で24時間、中・高リスク手技で48時間が望ましい。
脊椎穿刺
脊椎・硬膜外麻酔または穿刺を実施する場合、血栓塞栓性合併症の予防のために抗血栓薬で治療を受けている患者は、血腫を発症し長期間または永久的な麻痺を生じる危険がある。この危険性は特に手術後の硬膜外または髄腔内カテーテルの使用や止血に影響を与える薬剤の併用で増加する。
作用機序
アピキサバンは経口投与可能な高選択的可逆的第Xa因子直接阻害薬であり、遊離のまたは血塊に結合した第Xa因子に作用する。第Xa因子は凝固カスケードの最終段階でプロトロンビンをトロンビンに分解し、フィブリン塊形成を引き起こす。アピキサバンは血小板凝集には直接作用しないが、第Xa因子を阻害する事で間接的に、トロンビンによる凝血塊形成を減少させる。
承認取得状況
アピキサバンは欧州で2012年4月に承認された。
米国ではARISTOTLE臨床試験が2011年に完了した後に新薬承認申請(NDA)資料が提出され、2012年12月に心房細動患者の脳梗塞予防薬として承認された。2014年3月には、膝または股関節置換術後の深部静脈血栓症(DVT)および肺血栓塞栓症(PE)の予防薬として追加承認された。2014年8月にはさらに、DVTおよびPEの再発予防薬として承認された。
日本では2011年12月に「心房細動患者における脳卒中の発症抑制」について承認申請し、2012年12月に承認された。「静脈血栓塞栓症(深部静脈血栓症および肺血栓塞栓症)の治療および再発抑制」については2015年2月に承認申請し、同年12月に承認を取得した。