プロテオパチー
| プロテオパチー | |
|---|---|

| |
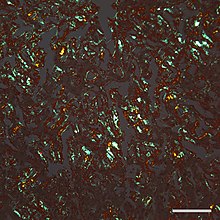
| 老人斑 (senile plaques) と脳アミロイドアンギオパチー (脳アミロイド血管症) に蓄積するタンパク質断片である「アミロイドβ」(Aβ)(茶色) に対する抗体で免疫染色した、アルツハイマー病患者からの大脳皮質の切片の顕微鏡写真。10倍顕微鏡対物レンズ。 |
医学では、プロテオパチー (proteopathy; プロテオパシーとも) ([proʊtiːˈɒpəθiː]; Proteo- [pref. protein]; -pathy [suff. disease]; proteopathies pl.; proteopathic adj) は、特定のタンパク質が構造的に異常になり、体の細胞、組織、臓器の機能を破壊する疾患のクラスを指す。多くの場合、タンパク質は正常な構成にフォールディング (折り畳み) できない。このミスフォールディング (誤った折り畳み) 状態では、タンパク質は何らかの方法で毒性になるか (毒性機能獲得)、または通常の機能を失う可能性がある。
プロテオパチー (proteopathies) (別名: プロテイノパチー (proteinopathies)、タンパク質構造障害 (protein conformational disorders)、またはタンパク質のミスフォールディング疾患 (protein misfolding diseases) として知られている) は、クロイツフェルト・ヤコブ病や他のプリオン病、アルツハイマー病、パーキンソン病、アミロイドーシス、多系統萎縮症、および他の疾患の広い範囲が含まれている(プロテオパチーのリストを参照)。プロテオパチー (proteopathy) という用語は、最初にラリー・ウォーカー (Lary Walker) とハリー・レヴィン (Harry LeVine) によって2000年に提案された。
プロテオパチーの概念は、その起源を19世紀半ばまで遡ることができ、1854年、ルドルフ・ウィルヒョウ (Rudolf Virchow) は、アミロイド (amyloid; デンプンのような) という用語を作り、セルロースに似た化学反応を示す大脳アミロイド小体の物質を説明した。1859年、フリードライヒ (Friedreich) とケクレ (Kekulé) は、「アミロイド」がセルロースからなるのではなく、実際にはタンパク質を豊富に含んでいることを示した。その後の研究では、多くの異なるタンパク質がアミロイドを形成し、それらは、コンゴーレッド染色後の偏光顕微鏡観察時の交差偏光下での複屈折性や、電子顕微鏡で観察されるフィブリル状 (繊維状) の超微細構造、という共通点を持っていることが示されている。しかし、いくつかの蛋白質性病変は複屈折を欠き、アルツハイマー病患者の脳内にアミロイドβ (Aβ) タンパク質がびまん性に沈着しているような古典的なアミロイド線維をほとんど含まないか、または全く含まない。さらに、罹患臓器の細胞に毒性があるのはオリゴマーとして知られている小さな非フィブリル性タンパク質の凝集体であり、フィブリル性形態のアミロイド原性タンパク質は比較的良性である可能性があるという証拠が明らかになった。
病態生理
ほとんどの場合、すべてのプロテオパチーではないにしても、3次元フォールディング (コンフォメーション)の変化により、特定のタンパク質がそれ自体に結合する傾向が高まる。この凝集形態では、タンパク質は除去 (clearance; クリアランス) に対する抵抗性があり、影響を受ける臓器の正常な能力を妨害する可能性がある。場合によっては、タンパク質のミスフォールディングにより、通常の機能が失われる。例えば、嚢胞性線維症は、嚢胞性線維症膜貫通調節因子 (CFTR) タンパク質の欠陥によって引き起こされ、筋萎縮性側索硬化症/前頭側頭葉変性症 (FTLD) では、特定の遺伝子調節タンパク質が細胞質内で不適切に凝集し、核内での通常の役割を実行できない。タンパク質は、ポリペプチド骨格として知られる共通の構造的特徴を共有しているため、すべてのタンパク質は、ある状況下でミスフォールドされる可能性がある。しかし、おそらく脆弱なタンパク質の構造的特異性のために、比較的少数のタンパク質のみがタンパク質変性疾患に関連している。例えば、通常はアンフォールド (折り畳まれていない) されているか、またはモノマーとして比較的不安定なタンパク質 (つまり、単一の非結合タンパク質分子) は、異常なコンフォメーションにミスフォールドする可能性が高くなる。ほぼ全ての場合において、疾患を引き起こす分子構成には、タンパク質のβシート二次構造の増加を伴う。いくつかのプロテオパチーにおける異常なタンパク質は、複数の3次元形状に折りたたまれることが示されている。これらの変性タンパク質構造は、それらの異なる病原性、生化学的、およびコンフォメーション特性によって定義される。これらはプリオン病に関して最も徹底的に研究されており、タンパク質株と呼ばれている。
プロテオパチーが発症する可能性は、タンパク質の自己組織化を促進する特定の危険因子によって増加する。これらは、タンパク質の一次アミノ酸配列の不安定化変化、翻訳後修飾 (過剰リン酸化など)、温度やpHの変化、タンパク質の生産量の増加、またはその除去 (クリアランス) の減少が含まれている。加齢は、外傷性脳損傷と同様に、強い危険因子である。老化した脳では、複数のプロテオパチーが重畳する可能性がある。例えば、タウオパチーとAβアミロイドーシス (アルツハイマー病の重要な病理学的特徴として共存する) に加えて、多くのアルツハイマー病患者は脳内にシヌクレイノパチー (レビー小体) を併発している。
シャペロンやコ・シャペロン (タンパク質のフォールディングを助けるタンパク質) が、加齢や蛋白質ミスフォールディング病において、タンパク質の毒性に拮抗し、タンパク質恒常性を維持しているのではないかという仮説が立てられている。
播種誘発(seeded induction)
いくつかのタンパク質は、疾患を引き起こすコンフォメーションに折り畳まれた同じ (または類似の) タンパク質への曝露によって、異常な集合体を形成するように誘導でき、これは「播種 (seeding)」または「許容テンプレート化 (permissive templating)」と呼ばれるプロセスである。このようにして、罹患したドナーから罹患組織抽出物を導入することにより、易罹患性宿主に疾患状態を引き起こすことができる。そのような誘導性プロテオパチーの最もよく知られている形態はプリオン病であり、これは、疾患を引き起こすコンフォメーションの精製プリオンタンパク質に、宿主生物を曝露することによって感染する可能性がある。現在、Aβアミロイドーシス、アミロイドA (AA) アミロイドーシス、およびアポリポプロテインA-IIアミロイドーシス、タウオパチー、シヌクレイノパチー、およびスーパーオキシドジスムターゼ-1 (SOD1)、ポリグルタミン、およびTAR DNA結合タンパク-43 (TDP-43) の凝集を含む、他のプロテオパチーが同様のメカニズムによって誘発されるという証拠がある。
これらの例のすべてにおいて、タンパク質の異常な形態自体が病原体であるように見える。場合によっては、あるタイプのタンパク質の沈着は、おそらくタンパク質分子の構造的相補性のために、βシート構造に富む他のタンパク質の集合体によって実験的に誘発されることがある。例えば、AAアミロイドーシスは、絹、酵母アミロイドSup35、大腸菌 (Escherichia coli) 由来のカーリー線維 (curli fibrils) などの多様な高分子によってマウスで刺激される。さらに、アポリポプロテインA-IIアミロイドは、βシートを豊富に含む様々なアミロイド原線維によってマウスで誘発され、脳タウオパチーは、凝集したAβを豊富に含む脳抽出物によって誘導される。また、プリオンタンパク質とAβとの交雑播種 (cross-seeding) の実験的証拠もある。一般に、このような異種播種は、同じタンパク質の破損した形態による播種よりも効率が悪い。
プロテオパチーのリスト
リンク先は英語版サイト。
治療
多くのプロテオパチーのための効果的な治療法の開発は、挑戦的である。プロテオパチーは、多くの場合、異なる原因から生じる異なるタンパク質が関与しているため、治療戦略はそれぞれの疾患に合わせてカスタマイズする必要がある。しかし、一般的な治療法としては、罹患した臓器の機能を維持し、疾患の原因となるタンパク質の形成を減少させ、タンパク質のミスフォールディングおよび/または凝集を防止し、またはそれらの除去の促進が含まれる。例えば、アルツハイマー病では、疾患関連タンパク質Aβを親タンパク質から遊離させる酵素を阻害することにより、疾患関連タンパク質Aβの産生を減らす方法が研究されている。別の戦略は、抗体を用いて能動的または受動的な免疫化によって特定のタンパク質を中和することである。いくつかのプロテオパチーでは、タンパク質オリゴマーの毒性作用を阻害することが有益な場合がある。アミロイドA (AA) アミロイドーシスは、血中のタンパク質 (血清アミロイドA、またはSAA呼ばれる) の量を増加させる炎症状態を治療することによって減少できる。免疫グロブリン軽鎖アミロイドーシス(ALアミロイドーシス)では、化学療法により、様々な体の臓器でアミロイドを形成する軽鎖タンパク質を作る血球の数を減らすことができる。トランスサイレチン (TTR) アミロイドーシス (ATTR) は、ミスフォールドされたTTRが複数の臓器に沈着することに起因する。TTRは主に肝臓で産生されるため、TTRアミロイドーシスは、一部の遺伝性症例では、肝移植により進行を遅らせられる可能性がある。TTRアミロイドーシスはまた、タンパク質の正常な集合体 (4つのTTR分子が結合して構成されているため、テトラマーと呼ばれる) を安定化させることによって治療できる。安定化により、個々のTTR分子が逃げたり、ミスフォールディングしたり、アミロイドに凝集するのを防ぐことができる。プロテオパチーのための他のいくつかの治療戦略が研究されているが、これには、低分子 (small molecule) および低分子干渉RNA (siRNA)、アンチセンスオリゴヌクレオチド、ペプチド、および人工免疫細胞などの生物学的医薬品が含まれる。場合によっては、複数の治療薬を組み合わせて効果を高めることもある。


