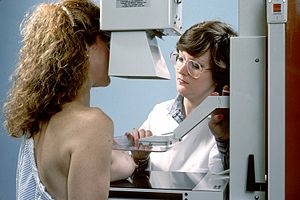
乳癌
| 乳癌 | |
|---|---|
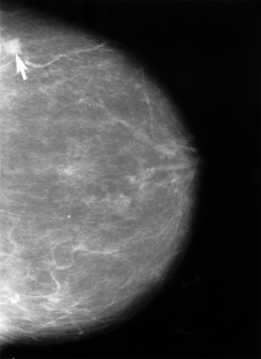 乳癌のX線画像(矢印)
| |
| 分類および外部参照情報 | |
| 診療科・ 学術分野 |
腫瘍学 |
| ICD-10 | C50 |
| ICD-9-CM | 174-175,V10.3 |
| OMIM | 114480 |
| DiseasesDB | 1598 |
| MedlinePlus | 000913 |
| eMedicine | med/2808 med/3287 radio/115 plastic/521 |
| Patient UK | 乳癌 |
| MeSH | D001943 |
| GeneReviews | |
乳癌(にゅうがん、英: Breast cancer、独:Brustkrebs、羅:Carcinoma mamae、略称:BC)とは、乳腺内の乳管および乳腺小葉の上皮由来の悪性腫瘍である。
40歳代後半から60歳代後半に多い。患者の大半は女性だが、男性にも女性の約1/100の頻度で発生する。
乳房の腫瘤(しこり)として発見されることが最も多い。
症状
女性
などの症状がみられる。
男性
- 男性の胸のしこりに関しては、「乳癌は男性には発生しない」と誤解する人が多いことから、女性に比べて発見・受診・治療開始が遅れる傾向がある。
- 男性では女性に比べ乳腺が表皮や胸壁に近接しているために、乳腺外への浸潤をきたしやすい。
- 男性の場合、乳癌の罹患時に同時に胸が異常発達(女性化乳房)の併発症状が見られることもある。
- 日本乳癌学会で2015年に新たに発症が登録された全(男女併せ)乳癌患者約8万7000人のうち、男性患者は560人であった。英国で乳癌に罹患した男性の患者の発生は、年辺り250人と報告されている。
女性乳癌と比べて症状や治療に関する情報が少ない、患者本人が乳癌を想定しないことが多い、女性の様にキャンペーン(ピンクリボンキャンペーン=乳癌啓蒙・乳癌検診の受診推進)を張っての乳癌検診や相談などの機会がほとんどないなどの理由から、NPO法人キャンサーネットジャパンが2018年から男性患者の交流会を開いている。
危険因子
乳癌の罹患率は様々な要因の影響を受ける。乳癌を発症しやすい遺伝的要因は複数知られている。また人種によっては乳癌リスクの高いグループが存在し、アジア系に比べてヨーロッパ系とアフリカ系は乳癌リスクが高い。
その他の危険因子としては以下のようなものが考えられている。
- 妊娠・出産歴がない。出産回数が少ない。
- 第一子出産の後、母乳を与えない。なお、関連がないとする報告もあり。
- 初経年齢(月経が始まった年齢)が低い。
- 閉経年齢が高い。
- ホルモン療法(エストロゲン製剤、ピルなど)を受けている。なお、関連がないとする報告もあり。
- 飲酒
- 喫煙(喫煙については、日本人を対象とした研究では、喫煙女性の乳癌リスクは、非喫煙者に比べて1.9倍となる。)
- 高脂肪の食事
- 20歳時の体重が低いほど乳癌になりやすい。閉経後の女性では、成人後の体重の増加が多いほど乳癌になりやすい。
- シフト勤務による不規則な生活(IARC(国際癌研究機関)は、「サーカディアン・リズムを崩すシフト勤務」をグループ2A(ヒトに対する発癌性がおそらくあるもの)と2010年に報告している。主に前立腺癌、乳癌のリスクを高める可能性があるとしている。)
- ホジキンリンパ腫治療のためのマントル照射の既往
- 女性化乳房(男性の場合)
- EBウイルス感染(インド・中国・北アフリカ・南ヨーロッパ にて、EBウイルスと乳癌との関連が指摘されていた。乳癌検体からのEBウイルス検出率としては約30%ほどである。2016年にはハーバード大学などの研究グループが、EBウイルスが乳腺上皮細胞に感染し、悪性形質転換させることを示している。)
年齢と共に乳癌の発生する確率は高まるが、若年齢で発生した乳癌は活動的である傾向が存在する。乳癌の一種の炎症性乳癌 (Inflammatory Breast Cancer) は特に活動的で、若い女性に多く、初診時のステージがIIIbまたはIVであることが多い。この癌はしばしばしこりを認めず、マンモグラフィーや超音波検査で発見することができない。乳腺炎 (Mastitis) のような乳房の炎症が症状として現れる。
遺伝的要因
全乳癌の約5~10%が遺伝性と考えられている。
BRCA1とBRCA2の2つの遺伝子は家族性乳癌と関連しており、遺伝性乳癌の9割に及ぶとされる。これらの遺伝子が発現している女性は、そうでない女性に比べて乳癌に罹患するリスクが極めて高い。これを「遺伝性乳癌卵巣癌(Hereditary Breast and Ovarian Cancer, HBOC)症候群」と呼ぶ。比較的若年で乳癌を発症し、しかもトリプルネガティブ乳癌であることが多い。このため日本では、HBOCが疑われる乳癌患者に対する遺伝子検査と、HBOCと診断され乳癌または卵巣癌を発症した患者に対する予防的手術は、2020年より一部が保険適応となっている。
他に乳癌と関連する疾患として、Li-Fraumeni症候群(p53遺伝子)、Cowden症候群(PTEN遺伝子)、Peutz–Jeghers症候群(STK11遺伝子)が知られており、その他にもCHEK2、ATM、BRIP1、PALB2遺伝子などの関連が知られている。
分類
乳癌は、非浸潤乳管癌 (ductal carcinoma in situ) 、非浸潤性小葉癌 (lobular carcinoma in situ) 、浸潤乳管癌 (invasive ductal carcinoma) に代表される浸潤癌、そしてパジェット病の4つに大別される。日本の乳癌取扱い規約では、浸潤乳管癌をさらに、乳頭腺管癌、充実腺管癌、硬癌の3つに細分類する。
検診
30歳代から高齢の女性ほど罹患率が高いため、今日では多くの国で検診を受けることが推奨されている。検診には胸部自己診断法 (breast self-examination) とマンモグラフィー (mammography) が含まれる。いくつかの国では、壮老年女性の全員の毎年のマンモグラフィー検診が実施され、早期乳癌の発見に効果を挙げている。ただし、検診にもデメリットは存在する。乳癌患者発見の背後には、その10倍以上の乳癌でない被験者が精密検査へと回り、生検(乳房に針を刺して細胞を採取する)を受けていることも事実である。こういったことから、2009年にはアメリカの予防医学作業部会が40歳代の定期的なマンモグラフィー検診は推奨しないと発表し、大きな議論となった。
マンモグラフィーは早期乳癌を発見するための選択肢の一つであり、それだけで全ての年齢層に対して、全ての乳癌の早期発見がカバーできるものではない。欧米では生涯乳癌リスクが20%以上の女性に対して造影剤を用いたMRIによるスクリーニングが推奨されている。日本では現在、40歳代における超音波検査の併用検診の効果について大規模な臨床研究が行われている。CTはX線被曝や費用の問題もあり、検診に用いられることは稀である。
20歳代での検査は、マンモグラフィー(描出率43%)よりも乳房超音波検査(描出率86%)が診断に有用である可能性が示唆された。これは、若年者では乳腺が発達しており、マンモグラフィーで高輝度乳腺となって、病変を検知することができないという経験論とも合致し、年齢に応じた検査法の選択が必要であることを強く示唆する。なお、高齢者では、乳腺が萎縮しているためマンモグラフィーでも病変の描出が比較的容易である。
マンモグラフィーでの30歳代の乳癌症例における2センチメートル以下の触知癌の感度は78%(40例中31例)と腫瘤に対する検出能力に関しては十分とはいえず、一方、超音波検査は触知腫瘤を全例検出していた。NCCNの乳癌スクリーニング・診断ガイドラインでは腫瘤を触知する30歳未満の患者では、画像診断として超音波検査施行を勧め,腫瘤を触知しない異常乳頭分泌のある患者には超音波検査±マンモグラフィーを勧めている。
マンモグラフィーにおける高濃度乳房では乳癌の発見が困難となる。高濃度乳房でのスクリーニングには、補完的にMRIを用いることで高率に乳癌を発見できるとの報告がある。
検査
壮老年女性の検診は増加しているにも関わらず、多くの女性が乳癌に最初に気づくのは、かかりつけ開業医などが乳房のしこりを発見したり、入浴中にしこりを自覚したりといった契機による。
一般的な乳癌のスクリーニング検査としては、問診、触診、軟X線乳房撮影(マンモグラフィー)、超音波検査などが実施される。臨床的に疑いが生じると、乳房MRI検査および細胞診や生検、マンモトームなどが実施され病理学的診断により癌であるかどうか判別される。マンモグラフィは簡便であるが、早期乳癌の検出率は56%であり、MRIの検出率92%に有意に劣るとされる。
細胞診は多くの場合、超音波装置の誘導で腫瘍内に細い針を挿入し腫瘍細胞を採取する。生検にはいくつかの種類があるが、超音波ガイド下にやや太目の針を挿入して腫瘍の一部を採取する針生検が最もスタンダードである。細胞診や針生検で診断が困難な場合には、超音波またはマンモグラフィーを取る機械を用いたマンモトーム生検、MRI検査でしか描出できない多発乳癌などの場合は、MRI検査をしながら生検を行うMRIガイド下乳腺生検が行われることもある。
マンモグラフィー
辺縁不正な腫瘤影、構築の乱れ、スピキュラ(spicula)、微細線状石灰化、微細分枝様石灰化が認められる。
- マンモグラフィー検診は、オランダにおいては乳癌による死亡を減少させなかった。またマンモグラフィ検診を受けなければ生涯を通じて検出されなかったであろう行き過ぎた乳癌過剰診断を増加させた。検診で見つかった乳癌の半数超(52%)は過剰診断乳癌と推定された。
- 米国での75歳以上のマンモグラフーィ検診では、0.80%に乳癌が発見された。76,885人の受診者のうち、616人に乳癌が認められ、82%の病変が浸潤性乳癌であり、17人の患者は高齢であるか、または健康状態に問題があり外科的加療を受けなかった との報告がある。
超音波検査
形状不整、内部エコー不均一、後方エコー減弱などが認められる。
CT
乳癌の診断がついた後、リンパ節や他臓器への転移の検索のために行われる。
MRI
乳癌の診断がついた後、乳癌の乳腺内への広がりの程度を知るために行われる。造影剤を使用してダイナミック撮影を行うのが一般的である。
腫瘍マーカー
以下のものなどが使用される。癌の再発を100%検知できるものでもなければ、例えばCEAは喫煙によって高値を示すなど、感度・特異度とも完全な検査ではないため、CTなどの術後の定期検査も必要となってくる。以下に参考値も付すが検査機器によって正常値が異なるため、検査値の評価するときには、それを確認する必要がある。
- CEA(癌胎児性抗原: carcinoembryonic antigen):2.5 ng/ml以下
- CA15-3(carbohydrate antigen 15-3):30 U/ml以下
病理診断
病理医は普通、腫瘍の組織型と、顕微鏡的なレベルの進行度合い(浸潤性であるか否か、など)を生検の報告に記述している。浸潤性乳癌のほとんどは腺癌(adenocarcinoma)であり、その中で最も普通の亜型は浸潤性乳管癌 (infiltrating ductal carcinoma ICD-O code 8500/3)である。他の亜型としては浸潤性小葉癌 (infiltrating lobular carcinoma ICD-O code 8520/3)、髄様癌(medullary carcinoma)、粘液癌(mucinous carcinoma)、管状癌(tubular carcinoma)、浸潤性微小乳頭癌(invasive micropapillary carcinoma)、化生癌(metaplastic carcinoma)などがある。稀に、腺癌以外の癌腫(あるいは癌腫以外の悪性腫瘍)がみられる。
また乳腺の増殖性病変の一部は乳癌と紛らわしい良性病変、良性と紛らわしい乳癌の顕微鏡像を呈することがあり、正しい診断に到達するためには、免疫染色という方法を用いることがある。乳腺病理専門医にたいしてセカンドオピニオンを求めたり、針生検においては無理に最終診断を下さず切除生検を推奨したりすることも、時に重要となってくる。
診断が確定すると、次は癌の病期の判定に移る。腫瘍の広がり具合と、浸潤や転移の有無を、病期判定の尺度とする。
病期
乳癌の病期(ステージ)は腫瘍の乳房内での広がり、リンパ節への転移の有無、癌細胞の遠隔転移で決まってくる。腫瘍の乳房内での広がりには、腫瘍のサイズ、皮膚や胸壁への浸潤の有無、炎症性乳癌という病態かどうかが含まれる。浸潤・転移が疑われリスクが高い場合は、CTスキャン、骨(シンチグラフィー)、フルオロデオキシグルコース陽電子断層撮影(FDG-PET)、磁気共鳴画像(MRI)、血液検査などの追加の検査で、遠隔転移の発見が試みられる。
| 病 期 | 解説 |
|---|---|
| 0期 | 非浸潤癌といわれる乳管内にとどまっている癌、または乳頭部に発症するパジェット病(皮膚にできる癌の一種)で、極めて早期の乳癌。 |
| I期 | しこりの大きさが2cm以下で、リンパ節や別の臓器には転移していない。 |
| IIA期 | しこりの大きさが2cm以下で、わきの下のリンパ節に転移があり、そのリンパ節は周囲の組織に固定されず可動性がある。または、しこりの大きさが2〜5cmでリンパ節や別の臓器への転移がない。 |
| IIB期 | しこりの大きさが2〜5cmで、わきの下のリンパ節に転移があり、そのリンパ節は周囲の組織に固定されず可動性がある。または、しこりの大きさが5cmを超えるが、リンパ節や別の臓器への転移がない。 |
| IIIA期 | しこりの大きさが5cm以下で、わきの下のリンパ節に転移があり、そのリンパ節は周辺の組織に固定されている状態、またはリンパ節が互いに癒着している状態、またはわきの下のリンパ節転移がなく胸骨の内側のリンパ節に転移がある場合。あるいは、しこりの大きさが5cm以上で、わきの下または胸骨の内側のリンパ節への転移がある。 |
| IIIB期 | しこりの大きさやリンパ節への転移の有無に関わらず、皮膚にしこりが顔を出したり皮膚が崩れたり皮膚がむくんでいるような状態。 |
| IIIC期 | しこりの大きさに関わらず、わきの下のリンパ節と胸骨の内側のリンパ節の両方に転移がある、または鎖骨の上下にあるリンパ節に転移がある。 |
| IV期 | 別の臓器に転移している。 |
※ 「国立がん研究センター がん情報サービス」の乳癌の病期(ステージ)分類表 より引用し改変。
治療
乳癌の治療は原則的には外科的切除であり、抗癌剤や抗エストロゲン剤など化学療法と放射線療法が併用される。術前に化学療法を行なうことをneo-adjuvant治療といい、術後に行なうことをadjuvant治療と呼ぶ。非浸潤性乳管癌の場合は、より集中的な治療を行うことでリスクを低減することができる。化学療法への腫瘍細胞の反応は様々で、術前化学療法で病理組織検査上、癌細胞が完全に死滅することもあるが、この場合でも、温存術後の放射線治療は省略すべきでないとされている。
外科手術
手術Stage I から III A に対して適応となる。最近では、乳房温存術と乳房切除術とでは予後に差がないことが報告されてきており、手術は拡大手術ではなく縮小手術が行われる傾向にある。
- 乳房温存術(lumpectomy - 腫瘤のみを摘出。乳腺腫瘤摘出術。)
- 乳房切除術(mastectomy - 乳房を切除ないし完全に切除する。)
- 胸筋合併乳房切除術
- 胸筋温存乳房切除術
腫瘤の大きさによって切除範囲が選択されるため、>3cm以上の大きな腫瘤や、胸壁や皮膚へ直接浸潤しているような進行している場合には広範囲切除となる。切除断端陽性(遺残)が再発の高リスクであるため、できる限りの腫瘤摘出が望まれる。
手術の際には、リンパ節郭清として、センチネルリンパ節生検 (sentinel lymph node biopsy) が行われ、リンパ節転移のある場合には状況によりセンチネルリンパ節のサンプリングだけで終わるか、腋窩リンパ節郭清を行なうか判断される。なお、乳房を直接切り開いて腫瘍を摘出する場合のほか、内視鏡を使用して摘出する場合もある。
根治的放射線療法 (radical radiation therapy)
乳房温存療法
温存術後に放射線治療を組み合わせた治療法を「乳房温存療法 (breast conservative treatment) 」といい、局所再発率といった治療成績は乳房全摘術 (amptation of the breast) と同等である。
乳房温存療法の禁忌
ただし妊娠中およびホモ接合性ATM遺伝子変異陽性例(極めてまれ)は放射線治療の絶対的禁忌である。また胸部照射の既往、活動性の強皮症や全身性エリテマトーデス (systemic lupus erythematosusをはじめとする膠原病の合併、二次性悪性腫瘍のリスクの高い遺伝性疾患の合併などは相対的禁忌とされる。また、放射線治療時には両手を挙上する必要があるがこの体位を保持できない場合にも、温存療法の適応とならない。
乳房温存療法の成績
乳房温存術後の局所再発の予防を目的とした乳房全照射が一般に行なわれ、術後照射により局所再発が1⁄3から1⁄4に減るとする文献もあり、大規模な研究によれば、生存期間を延ばすという効果も認められている。
照射野
照射野は通常、患側乳房全体であるが、腋窩リンパ節転移が主に4個以上あれば、鎖骨上窩リンパ節領域への予防照射も検討され、術前の画像上、胸骨傍リンパ節転移を疑う場合には同部位も照射野に入れる。
乳房温存術後の予防照射としては、全乳房に対して50Gy/25fr(一回に2Gy(グレイ)という放射線量を25回照射し、総線量50Gy照射)照射するのが、一般的である。術後断端が陽性(顕微鏡レベルではあるが、手術で癌を取り切れていなかった可能性が高い)である場合などは、癌が元あった場所(腫瘍床)に10Gy/5fr追加で照射することもある(ブースト照射)。
乳房全切除術後放射線療法(postmastectomy radiation therapy; PMRT)
乳房全切除術後の放射線療法はPMRTと呼ばれる。腋窩リンパ節転移4個以上の場合はPMRTが標準治療であり、1~3個の場合もPMRTが推奨されるが全例に行うべきかどうかは議論の余地がある。照射野は胸壁および鎖骨上リンパ節領域(±内胸リンパ節領域)となり、郭清したリンパ節への照射は推奨されない。
早期有害事象
術後の予防照射では、皮膚の発赤や茶褐色の着色、乾燥、かゆみ、術創部付近のぴりぴり感などの急性の有害事象が生じることが多いものの、概して軽度に治まり、徐々に(一年程度)、照射による変化は消失していく。
晩期有害事象
一方、患側の手の浮腫は手術によるリンパ節郭清の影響と相俟って、強く出ることもあり、これは鎖骨上窩リンパ節照射を照射することによって、出現頻度が高まり、まだ症状も強い傾向にある。一旦浮腫が起こると治療することが難しいため、ならないように生活指導されるが、重いものを持たないなど患側の手を愛護的に扱うといったことが中心である。しかし、患側が利き手であるとこうしたことは難しく、研究結果とともに患者の今後の生活まで視野に入れた治療方針を決定することが重要である。また、左乳癌の場合、心臓もわずかに照射野に入るため、心膜炎、狭心症、心筋梗塞といった有害事象も生じうる。さらに、放射線による二次発癌も懸念される。
治療スケジュール
25回の照射は、通常土曜日、日曜日、祝日を除いて毎日連続で行なうことが必要であり、一か月と少しは毎日病院に来る必要があって、通院が負担となる例もある。そのため短期照射といって、25回よりも短い期間で同様の効果が得られる放射線治療法が健康保険でも認められており、利用されている。ただし、短期照射では、総線量が50Gyに満たない。民間の医療保険では、放射線治療を行なった場合、50Gy以上の照射でなければ、保険金が出ないという契約となっていることも多く、短期照射を希望する場合は確認が必要である。
また、小線源治療などにより、乳房全体ではなく、腫瘍があった部分に限局して放射線を照射するという研究もなされており、結果が待たれる。
緩和的放射線治療 (palliative radiation therapy)
転移および再発における症状緩和を目的とした照射がある。乳癌は比較的骨転移を来しやすい癌腫である。骨転移は無症状の場合もあるが、強い疼痛を伴うこともあり、こうした場合に病変部に照射すると、9割程度で除痛効果が得られ、半数では完全に痛みが消失する。背骨(脊椎)に転移すると、脊髄という神経の束を圧迫して、麻痺などを起こすこともあるが、放射線照射で癌を制御することにより、麻痺が解除されうる。また、脳転移も時に認められるが、数が少なければ定位放射線治療を行なったり、多ければ全脳照射を行なったりする。
他、肝臓や、肺にも転移しやすく、少数であれば定位放射線治療の適応もあるが、一般に化学療法などの全身療法をすることが多い。転移には血管新生も関係している。腫瘍の血管新生はがん細胞が周りの正常組織にPI3K/Akt/mTORシグナルを送ることから始まる。このシグナルは、正常組織の特定の遺伝子の発現をうながし、それによって新しい血管が作られる。このシグナルの働きを阻害することで、がん細胞の増殖や転移を抑制すると考えられている。
化学療法
ホルモン受容体の発現の有無、HER2発現の有無、Ki-67発現、遺伝子発現プロファイリングなどに応じて、内分泌薬、抗癌剤、分子標的治療薬の3種類が組み合わせて用いられる。
化学療法は周術期に行うものと転移・再発例に行うものに分けられる。前者は根治を目指した治療で、後者は延命・QOL向上を目指した治療である。前者において術前化学療法と術後化学療法の効果は同等であるとされ、症例によってどちらかが選択される。乳房温存手術を希望する場合は術前化学療法が選択されることが多い。
- 内分泌薬
- 乳癌はエストロゲン依存性であることが多いことから、エストロゲン受容体 (ER) 、プロゲステロン受容体 (PgR) の発現の高いものは内分泌薬が奏効する。
-
閉経前後で以下の通りに行われる。
- 閉経前女性:抗エストロゲン薬±LH-RH作用薬
- 閉経後女性:アロマターゼ阻害薬または抗エストロゲン薬
- 抗癌剤
- 以下の通りに行われる。
- 分子標的治療
- ヒト上皮成長因子受容体2 (HER2) 陽性の場合、分子標的治療薬が奏効する。
-
BRCA1/2変異陽性の場合、PARP阻害薬が奏効する。
- オラパリブ : PARP阻害剤
- mTOR阻害剤
- CDK4/6阻害薬
- 抗PD-L1抗体
- アテゾリズマブ
周術期薬物治療
化学療法
浸潤性乳癌に対して術前または術後にアンスラサイクリンベースのレジメンとタキサン系薬剤の逐次投与が行われる。再発リスクが高く、骨髄機能が良好な場合はG-CSFを併用したdose dense化学療法が推奨される。再発リスクが高いと判断される場合にはUS Oncology 01062試験およびFinXX試験の結果からカペシタビンの併用も検討する。
アンスラサイクリンまたはタキサンによる術前化学療法でpCRが得られなかった場合には、CREATE-X試験の結果から術後にカペシタビンの併用も検討される。
ホルモン受容体陽性で遺伝子発現プロファイルから再発リスクが低いと判断される場合には化学療法を省略して内分泌療法のみとなる場合もある。
HER2が陽性の場合の治療は別項で記載する。
ホルモン受容体陽性乳癌に対する内分泌療法
ホルモン受容体陽性乳癌に対しては術後内分泌療法が推奨されている。閉経前後で体内のエストロゲンの主要な産生源が異なることから、推奨される薬剤が異なっている。閉経前の場合は抗エストロゲン薬であるタモキシフェンが基本となり、症例によってLH-RHアゴニストの上乗せが検討される。閉経後の場合はアロマターゼ阻害薬が推奨されている。
術後内分泌療法の期間としては5年投与と10年投与の比較で後者が優れているため、再発リスクと副作用を考慮した上で10年投与が推奨される。
HER2陽性乳癌に対する抗HER2療法
術前または術後に、薬物治療が行われる。細胞障害性薬剤に加えてトラスツズマブの合計1年間の投与が推奨される。再発リスクの高い場合にはAPHINITY試験の結果から、トラスツズマブに加えてペルツズマブの併用も推奨される。
またトラスツズマブを含む術前化学療法でpCRが得られなかった場合にはKATHERINE試験の結果からT-DM1の投与が行われる。
転移・再発例への薬物治療
化学療法
エストロゲン受容体、プロゲステロン受容体、HER2受容体のどれかが陽性の内腔細胞乳癌と、これら3つの受容体を全くもたないトリプルネガティブ乳癌があり、トリプルネガティブ乳癌は全乳癌の約20%を占める。 これら3つの受容体があると、ホルモン療法や抗体療法などの分子標的療法で癌を抑制できるが、トリプルネガティブ乳癌はこれらのいずれの受容体ももたないため、有効な分子標的療法がなく、また浸潤・転移もしやすいことから、乳癌の中でも最も予後が不良である。 化学療法はトリプルネガティブ乳癌に対する標準治療となる。またホルモン受容体陽性乳癌に対しては通常内分泌療法が行われるが、病勢が急速に進行する場合や内分泌療法耐性の場合は化学療法が行われる。
一次治療としてはアンスラサイクリン系薬剤を含むレジメン、タキサン系薬剤が強く推奨され、TS-1単剤が弱く推奨される。PD-L1陽性のトリプルネガティブ乳癌に限り、IMPASSION130試験の結果に基づきナブパクリタキセル+アテゾリズマブの併用療法が選択肢となる。二次治療では一次治療で用いなかったレジメンに加えて、カペシタビン、エリブリンが強く推奨され、ゲムシタビン、ビノレルビンが弱く推奨される。一次治療および二次治療において、化学療法にベバシズマブを併用することも検討される。三次治療以降は、一次治療および二次治療で用いられなかった薬剤が投与される。トリプルネガティブ乳癌に限りプラチナ製剤も選択肢となり弱く推奨されるものの、トリプルネガティブ乳癌に対する保険適応を有していないことに注意が必要となる。
BRCA1/2遺伝子変異陽性の場合、アンスラサイクリンおよびタキサンを投与した後の治療としてオラパリブの使用が推奨される。
ホルモン受容体陽性乳癌に対する内分泌療法
閉経前の場合は一次治療としてタモキシフェン+卵巣機能抑制(多くの場合LH-RHアゴニスト)が強く推奨される。二次治療としてはLH-RHアゴニスト+フルベストラント+CDK4/6阻害薬または卵巣機能抑制の上で閉経後に用いる薬物治療を行うことが弱く推奨される。
閉経後の一次治療は非ステロイド性アロマターゼ阻害薬+CDK4/6阻害薬が強く推奨され、フルベストラント単剤および非ステロイド性アロマターゼ阻害薬単剤は弱い推奨となっている。一次治療として非ステロイド性アロマターゼ阻害薬+CDK4/6阻害薬を投与した場合の二次治療に投与すべき薬剤は確立しておらず、一次治療で未使用の薬剤が考慮される。一次治療で非ステロイド性アロマターゼ阻害薬単剤を用いた場合は、二次治療としてフルベストラント+CDK4/6阻害薬の投与が推奨され、三次治療以降はエキセメスタン+エベロリムスや、一次および二次治療で用いられていない薬剤の投与が行われる。
HER2陽性乳癌に対する抗HER2療法
一次治療はCLEOPATRA試験の結果からドセタキセル+トラスツズマブ+ペルツズマブが標準治療であるが、トラスツズマブエムタンシン、トラスツズマブ+化学療法も弱く推奨される。二次治療はEMILIA試験の結果からトラスツズマブエムタンシンが標準治療だが、トラスツズマブ+化学療法も弱く推奨される。三次治療以降としてDESTINY breast01試験の結果からトラスツズマブデルクステカンが推奨されるが、間質性肺疾患に注意する。トラスツズマブ+化学療法も弱く推奨される。
化学療法の適応とならない且つホルモン受容体陽性の場合は、抗HER2療法と内分泌療法の併用が推奨され、内分泌療法単独は推奨されない。
予後
乳癌の治療成績は、診断確定時の病期と治療内容に依存する。一般に、発見および治療開始が早いほど予後は良い。早期であればほとんどの乳癌が手術によって根治する。
外科的手術を行った場合、審美的な観点および患者の精神的なケアの観点から、乳房再建術が行われることがある。さらに再建後の乳房に適したブラジャーの相談対応やオーダーメイドも行われている。
男性乳癌では女性乳癌と比較して大胸筋浸潤を起こしやすく、進行癌で発見される確率が高いため、5年生存率40〜50%と予後不良であると考えられてきた。米国ヴァンダービルト大学医療センターの調査報告によれば、乳癌に罹患した患者の生存率には性別による差違があり、乳癌に罹患した患者は「男性の方が死亡率は高い」と報告されている。しかしながら、女性患者と比べて全生存率、無病生存率ともに変わらないという報告もある。
5年生存率は、米国と英国イングランドでは80%から90%であった。途上国においては5年生存率は低い。2018年には200万人が新たに発症し、627,000人が死亡した。
乳癌は、他の癌に比べて長期間経過後の再発が多いため、術後10年間の経過観察が一般的である。
予防
乳癌の予防の可能性の要素として次のようなものがある。
- 余暇運動への参加が多いほど、乳癌になりにくい。総身体活動量が高い女性は、閉経後においてホルモン受容体陽性の乳癌になりにくい。過体重の女性では、週1回以上の余暇運動に参加する人は、乳癌になりにくい。
- 大豆イソフラボンであるゲニステインの血中濃度が高いグループの乳癌リスクは低い。味噌汁の摂取が多いほど、乳癌になりにくい。大豆イソフラボンは乳癌発生率減少と関連している。
- 総野菜・総果物摂取量全体では、乳癌発生との関連は観察されなかったが、閉経前の女性では、「アブラナ科野菜」の摂取量が高いほど、乳癌になりにくいとの報告がある。
- 閉経前女性では、マメ科植物、家禽類、ナッツ、魚類の摂取合計が、獣肉(レッド・ミート)摂取に対して多いと、乳癌の相対リスク低下が見られた。
疫学
世界中でよく見られる癌で、西側諸国では女性のおよそ10%が一生涯の間に乳癌罹患する機会を有する。それゆえ、早期発見と効果的な治療法を達成すべく膨大な労力が費やされている。
日本でも女性の全癌において罹患数第1位であり、増加傾向にある。生涯で乳癌に罹患する確率は、日本人女性で16人に1人、欧米では8~10人に1人である。一方、死亡数は2021年の女性の全癌死亡の第4位である。
また大阪府癌登録による成績では、1975 - 2001年に診断された乳癌全罹患数(39,879例)のうち、男性乳癌は0.57%(226例)であった。また、Tajimaらは、男性乳癌の最頻値が60歳代であることを示した。
乳癌に罹患するリスクは年齢と共に増加する。
| 年齢 | 総患者数 | 男性 | 女性 |
|---|---|---|---|
| 0歳 | 0 | 0 | 0 |
| 1-4 | 0 | 0 | - |
| 5-9 | - | - | - |
| 10-14 | 0 | 0 | - |
| 15-19 | 0 | - | 0 |
| 20-24 | 0 | 0 | 0 |
| 25-29 | 1 | 0 | 1 |
| 30-34 | 2 | - | 2 |
| 35-39 | 5 | 0 | 5 |
| 40-44 | 11 | 0 | 11 |
| 45-49 | 24 | 0 | 24 |
| 50-54 | 26 | 0 | 26 |
| 55-59 | 23 | 0 | 23 |
| 60-64 | 26 | 0 | 26 |
| 65-69 | 33 | 0 | 33 |
| 70-74 | 26 | 0 | 26 |
| 75-79 | 24 | 1 | 23 |
| 80-84 | 16 | 0 | 16 |
| 85-89 | 10 | 0 | 9 |
| 90歳以上 | 5 | 0 | 5 |
| 不詳 | 0 | - | 0 |
| 合計 | 232 | 3 | 229 |
(厚生労働省平成29年患者調査による)
転移
乳癌は肺、骨、脳、副腎、肝臓への転移が多い。乳癌の骨転移の頻度は57〜73%である。
歴史
乳癌は古代からあった病気で、古代エジプトにおいてはイムフォテプと言う医師による乳癌治療の記録がパピルス文書に残されている(紀元前3000年 - 紀元前5000年のこと)。
古代における乳癌の主な治療方法は、乳房の一部を切開することで悪性腫瘍を排膿し、残りの腫瘍は原始的に焼却したり腐敗させたりした。古代においては麻酔も防腐もない時代であるので、乳癌の手術には大変な苦痛が伴い、手に負えないものであれば軟膏を塗るといった姑息的な手法によるしかできなかった。
それから長い時代において、乳癌治療の歴史 は停滞したままであったが、16世紀にアンブロワーズ・パレという外科医が、糸による結紮(けっさつ)で細胞を壊死させ、それによって癌を取り除くという手法を試みた。乳癌の手術技法を確立したのは、フランスの外科医、ジャン=ルイ・プティ(1674年 - 1750年)である。その方法は、癌に周囲組織を大きく付けて一塊にして切り取り、さらに転移を防ぐために腋窩リンパ節を取るものであり、これは現代の外科の考えと一致するものである。彼の死後24年後にはその業績は出版され、1800年代に入ってからは多くの外科医が乳癌治療の腕を競うようになった。
1804年には、華岡青洲(花岡青州)が全身麻酔下において、乳癌摘出手術に成功した。
今日の乳癌手術の術式を確立したのはW・S・ハルステッドであり、1970年代まで彼の確立した術式は世界中で認められ、用いられるようになった。ハルステッドは1882年、最初の根治的乳房切断手術を行った。これまでの手術と違う所は、癌腫瘤から大きく離して正常皮膚乳腺組織を大きく癌の癌腫瘤の側に付けて切除し、さらに大胸筋と腋窩リンパ節を摘除していることである。
メイヤーは1894年、6例の根治的乳房切断術を行ったことを報告している。彼は大胸筋のみでなく、より安全を確保するために小胸筋も切除した。こうして乳癌根治術方が確立されることとなった。乳癌は乳房を切除しても皮膚は腋窩に癌が再発することが多かったが、ハルステッドの療法によって、それまでの再発率60%から70%が6%に劇的に抑えられるようになった。
脚注
参考文献
- 日本乳癌学会 編 編『科学的根拠に基づく 乳癌診療ガイドライン2004年版』金原書店、2004年7月。ISBN 978-4307201902。http://minds.jcqhc.or.jp/n/med/4/med0006/G0000226/0001。
- 乳癌診療ガイドライン2018年版
関連項目
- 腫瘍学
- 悪性腫瘍
- 産婦人科学
- 華岡青洲 - 1804年に世界初の全身麻酔下における乳癌摘出手術を実施。
- ピンクリボン - 乳癌やその検診に関する世界規模の啓発キャンペーン。
- 余命一ヶ月の花嫁 - 24歳で末期の乳癌と診断された一般女性のドキュメンタリー番組。
- 癌の一覧
- がん予防研究
乳癌が原因で逝去した主な著名人
- 中城ふみ子 - 乳癌罹患後に『乳房喪失』と題した歌集を発表した歌人。
- 武原英子 - 女優。錦野旦の前妻。
- 田中好子 - キャンディーズの元メンバー。再発を含め19年間の闘病生活を送り、死後に「田中好子最後の180日」というドキュメンタリー番組が公開された。
- 水谷優子 - 声優。テレビアニメ『ちびまる子ちゃん』のお姉ちゃん(さくらさきこ)役などを務めた。
- 川村カオリ - ロック歌手。
- 小林麻央 - 元フリーアナウンサー、キャスター。十一代目市川海老蔵の妻。
- さくらももこ - 漫画『ちびまる子ちゃん』の原作者。
- 久野綾希子 - 元劇団四季所属のミュージカル女優。
外部リンク
- “乳がんの情報”. がん情報サイト Cancer Information Japan. 先端医療振興財団 臨床研究情報センター. 2015年3月11日閲覧。 - 米国国立がん研究所が発行するPDQ(Physician Data Query)の日本語版。
- 乳癌 - MSDマニュアル
(関連団体)
- “一般社団法人 日本乳癌学会”. 2023年1月2日閲覧。
- “国立研究開発法人 国立がん研究センター”. 2023年1月2日閲覧。
- “公益財団法人 がん研究会”. 2023年1月2日閲覧。
- “公益財団法人 日本対がん協会”. 2023年1月2日閲覧。
- “特定非営利活動法人 日本乳がん検診精度管理中央機構”. 2023年1月2日閲覧。
- 乳癌 - 国立がん研究センター がん情報サービス 一般の方向けサイト。2023年1月2日閲覧。
- 乳癌 - 慶應義塾大学病院 医療・健康情報サイト、2023年1月2日閲覧。