Folding@home

| |
| 作者 | ビジェイ・S・パンデ |
|---|---|
| 開発元 | Pande Laboratory, ソニー, NVIDIA, ATI, Joseph Coffland, Cauldron Development |
| 初版 | 2000年10月1日 (2000-10-01) |
| 最新版 |
7.6.21
/ 2020年10月23日 (2020-10-23)
|
| 対応OS | Microsoft Windows, macOS, Linux |
| プラットフォーム | IA-32, x86-64, ARM |
| 対応言語 | 英語 |
| 種別 | 分散コンピューティング |
| ライセンス | プロプライエタリ |
| 公式サイト | foldingathome.org |
Folding@home(フォールディング・アット・ホーム、FAH、F@hとも呼ばれる)は、タンパク質の動的なふるまいをシミュレートすることで、科学者が様々な疾患に対する新しい治療法を開発できるよう支援することを目的とした分散コンピューティングプロジェクトである。
これにはタンパク質のフォールディングやタンパク質の動きのプロセスが含まれており、ボランティアのパソコン上で実行される分子動力学シミュレーションに依存している。Folding@homeは、2000年10月1日にビジェイ・パンデ教授の指揮のもと、スタンフォード大学で発足した。2019年以降は、セントルイス・ワシントン大学医学部に拠点を置き、パンデ教授の元教え子であるグレッグ・ボーマン博士が指揮している。
このプロジェクトは、分散コンピューティングや科学研究を行うために、グラフィックス処理装置(GPU)、中央処理装置(CPU)、Raspberry PiのようなARMプロセッサを利用する。このプロジェクトでは、従来のコンピューティング手法からパラダイムシフトした統計的シミュレーション手法を採用している。クライアント・サーバモデルのネットワーク・アーキテクチャの一環として、ボランティアのマシンはそれぞれシミュレーションの一部(ワークユニット、WU)を受け取り、計算により完成させ、プロジェクトのデータベースサーバに返し、そこでユニットが全体のシミュレーションにまとめられる。ボランティアは自分の貢献度をウェブサイト「Folding@home」上で確認することができるため、参加に競争心を刺激し、長期的な貢献を促している。
Folding@homeは、世界最速の計算機システムの一つである。COVID-19パンデミックの影響でプロジェクトへの関心が高まる中、2020年3月下旬には本プロジェクトの演算能力は約1.22 E(エクサ)FLOPS(フロップス)、2020年4月中旬には約2.43 EFLOPSを達成し、世界初のエクサフロップ・コンピューティング・システムとなり、TOP500の全スーパーコンピュータの合算を上回る能力を獲得した。 研究者は、計算コストのかかるタンパク質の折りたたみに関する原子レベルのシミュレーションを、従来の数千倍の長い時間に渡って実行することが可能となった。Pande Labは、2000年10月1日の発足以来、225の科学研究論文を発表してきた。このプロジェクトのシミュレーション結果は、実験の結果とよく一致している。
背景
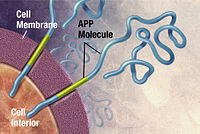
タンパク質は、多くの生物学的機能に不可欠な構成要素であり、生物細胞内の事実上すべてのプロセスに関与している。 タンパク質は多くの場合、酵素として機能し、細胞のシグナル伝達、分子輸送、細胞周期の制御などの生化学反応を行っている。 構造要素として、いくつかのタンパク質は、細胞の骨格の一種である抗体として機能し、他のタンパク質は免疫システムに関与している。 タンパク質がこれらの役割を果たす前に、タンパク質は機能的な三次元構造に折りたたまれなければならない。 このプロセスは、しばしば自然発生的に行われ、アミノ酸配列内の相互作用やアミノ酸とその周囲のアミノ酸との相互作用に依存する。 タンパク質の折り畳み(フォールディング)は、タンパク質の最もエネルギー的に有利な構造、すなわち天然状態(立体配座)を見つけるための探索によって推進される。 このように、タンパク質のフォールディングを理解することは、タンパク質が何をしているのか、どのように機能しているのかを理解する上で非常に重要であり、計算生物学の聖杯と考えられてる。 フォールディングは、混雑した細胞環境の中で行われているにもかかわらず、通常はスムーズに行われている。 しかし、タンパク質の化学的性質やその他の要因により、タンパク質が誤って折り畳まれ(ミスフォールディングと呼ばれる)、誤った経路で折りたたまれてしまい、形が崩れてしまうことがある。 誤って折り畳まれたタンパク質を細胞のメカニズムで破壊したり、再フォールディングしたりしない限り、タンパク質はその後凝集し、様々な消耗性疾患を引き起こす可能性がある。 これらのプロセスを研究する実験室での実験は、範囲や原子レベルでの詳細が限られているため、科学者たちは、物理学に基づいた計算モデルを使用して実験を補完し、タンパク質のフォールディング、ミスフォールディング、凝集のより完全な全体像を提供しようとしている。
タンパク質の立体配座やコンフィギュレーション空間(タンパク質が取り得る形状のセット)の複雑さと計算能力の限界から、全原子分子動力学シミュレーションでは研究できるタイムスケールが大幅に制限されている。 ほとんどのタンパク質は通常ミリ秒単位で折りたたまれるのに対して、2010年以前のシミュレーションではナノ秒からマイクロ秒のタイムスケールにしか到達できなかった。 タンパク質のフォールディングのシミュレーションには、汎用スーパーコンピュータが使用されてきたが、このようなシステムは本質的にコストが高く、多くの研究グループで共有されているのが一般的であった。 さらに、動力学モデルの計算は連続的に行われるため、従来の分子シミュレーションをこれらのアーキテクチャに強スケーリングすることは非常に困難といえる(問題の大きさに対して多数のプロセッサを適応することが難しくなる)。 さらに、タンパク質の折りたたみは確率的なプロセス(すなわちランダム)であり、時間の経過とともに統計的に変化する可能性があるため、折りたたみプロセスを包括的に見るために長時間のシミュレーションを行うことは計算的に困難であった。
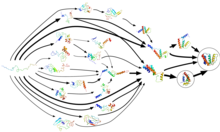
タンパク質のフォールディングは一度に起こるものではない。 その代わりに、タンパク質は、タンパク質のエネルギー地形における局所的な熱力学的自由エネルギーの最小値である様々な中間的な構造の状態で待機している間に、フォールディングに時間の大部分を費やしている(場合によっては96%近く)。 適応的サンプリングとして知られるプロセスを通じて、これらの立体配座はFolding@homeによって、一連のシミュレーション軌道の出発点として使用される。 シミュレーションがより多くの立体配座を発見すると、それらの立体配座から軌道が再開され、この周期的なプロセスからマルコフ状態モデル(MSM)が徐々に作成される。 MSMは離散時間マスター方程式モデルであり、生体分子の構造とエネルギーランドスケープを、異なる構造とその間の短い遷移の集合として記述する。 適応サンプリングマルコフ状態モデル法は、局所的なエネルギー最小値自体の内部での計算を避けることができるため、シミュレーションの効率を大幅に向上させ、短い独立したシミュレーション軌道の統計的集約を可能にするため、分散コンピューティング(GPUGRIDを含む)に適している。 マルコフ状態モデルの構築に要する時間は、並列シミュレーションの実行回数、すなわち利用可能なプロセッサの数に反比例する。 言い換えれば、線形並列化を実現し、全体の直列計算時間を約4桁短縮することができる。 完成したMSMには、タンパク質の相空間(タンパク質がとることのできるすべての立体配座)とその間の遷移のサンプル状態が数万個含まれている場合がある。 このモデルはフォールディングイベントとフォールディング順序(すなわち経路)を示しており、研究者は後で動力学的クラスタリングを使用して、そうでなければ非常に詳細なモデルの粗視化された表現を見ることができる。 これらのMSMを用いて、タンパク質がどのようにして誤って折りたたまれるかを明らかにし、シミュレーションと実験を定量的に比較することができる。
2000年から2010年の間に、Folding@homeが研究してきたタンパク質の長さは4倍に増加し、タンパク質フォールディングシミュレーションのタイムスケールは6桁に増加した。 2002年には、Folding@homeはマルコフ状態モデルを使用して数ヶ月間で約100万CPU日分のシミュレーションを行い、2011年にはMSMの並列化を行い、合計1000万CPU時間の計算を必要とした。 2010年1月には、Folding@homeはMSMを使用して、1.52ミリ秒の間に32残基のNTL9タンパク質がゆっくりと折りたためる動力学のシミュレーションを行った。 このモデルは、実験的なフォールディング速度の予測と一致するタイムスケールでありながら、以前に達成されたものよりも千倍も長いものであった。 このモデルは、それぞれが2桁も短い多数の個別の軌道から構成されており、タンパク質のエネルギー地形をこれまでにないレベルで詳細に調べることができた。 2010年、Folding@homeの研究者であるグレッグ・ボーマン(Gregory Bowman)は、オープンソースのMSMBuilderソフトウェアの開発と理論と実験の定量的な一致を達成したことにより、米国化学会からトーマス・クーン(Thomas Kuhn)パラダイムシフト賞を受賞した。 彼の研究に対して、パンデ(Pande)は、「タンパク質とRNAのフォールディングに関する最先端の理論モデルを生み出すために、分野を定義し、分野を変える計算手法を開発した」として、2012年にMichael and Kate Bárány Award for Young Investigatorsを、また、「アンサンブル測定と単一分子測定の両方の意味の再検討を刺激し、パンデの努力はシミュレーション方法論への先駆的な貢献となった」として、2006年にはIrving Sigal Young Investigator Awardを受賞している。
生物医学研究への応用例
タンパク質の誤った折り畳み(ミスフォールディング)は、アルツハイマー病、癌(がん)、クロイツフェルト・ヤコブ病、嚢胞性線維症、ハンチントン病、鎌状赤血球性貧血、およびII型糖尿病を含む様々な疾患の原因となり得る。 HIVやインフルエンザなどのウイルスによる細胞感染には、細胞膜上でのタンパク質のフォールディング現象も関与している。 タンパク質のミスフォールディングがよりよく理解されれば、タンパク質のフォールディングを調節する細胞の自然な能力を増強する治療法を開発することができる。 このような治療法には、特定のタンパク質の産生を変化させたり、ミスフォールディングしたタンパク質を破壊したり、あるいはフォールディングプロセスを補助するために人工分子を使用することが含まれる。 計算分子モデリングと実験解析の組み合わせは、創薬の迅速化やコスト削減など、分子医学の未来と合理的な医薬品設計法を根本的に形作る可能性を秘めている。 Folding@homeの最初の5年間の目標は、フォールディングの理解を前進させることであったが、現在の目標は、ミスフォールディングと関連疾患、特にアルツハイマー病の理解である。
Folding@home上で実行されるシミュレーションは、実験室での実験と併用されるが、研究者はこれらのシミュレーションを利用して、実験室環境(in vitro)でのフォールディングが、本来の細胞環境でのフォールディングとどのように異なるのかを研究することができる。 これは、実験的に観察することが困難なフォールディングやミスフォールディング、そしてそれらと疾患との関係を研究する上で有利である。 例えば、2011年のFolding@homeでは、リボソーム出口トンネル内でのタンパク質のフォールディングをシミュレーションし、自然の閉じ込めや混雑がフォールディングプロセスにどのような影響を与えるかを、科学者が理解するのに役立てた。 さらに、科学者は通常、化学的変性剤を働かせ、タンパク質を安定なネイティブ状態からアンフォールド(展開)させている。 変性剤がタンパク質の再フォールディングにどのような影響を与えるかは一般的には知られておらず、これらの変性状態に、フォールディングの挙動に影響を与える可能性のある残余構造が含まれるかどうかを実験的に判断することは困難である。 2010年にFolding@homeは、GPUを使ってプロテインLの未フォールディング状態をシミュレーションし、実験結果と強く一致する崩壊速度を推定した。
このプロジェクトから得られた大規模なデータセットは、要求に応じて他の研究者が自由に利用できるようになっており、Folding@homeのウェブサイトからアクセスできるものもある。 パンデ研究室は、Blue Geneスーパーコンピュータのような他の分子動力学システムと協力しており、Folding@homeの主要なソフトウェアを他の研究者と共有していて、Folding@homeの恩恵を受けたアルゴリズムが他の科学分野に役立つ可能性がある。 2011年には、Folding@homeのMSMやその他の並列化手法をベースに、大規模なコンピュータクラスタやスーパーコンピュータ上での分子シミュレーションの効率とスケーリングを向上させることを目的としたオープンソースのCopernicusソフトウェアをリリースした。 Folding@homeで得られたすべての科学的知見の要約は、発表後にFolding@homeのウェブサイトに掲載される。
アルツハイマー病
アルツハイマー病は、高齢者に多く発症し、認知症の半数以上を占める難治性の神経変性疾患である。 正確な原因は不明だが、この病気はタンパク質のミスフォールディング疾患として同定されている。 アルツハイマー病は、アミロイドβペプチド(Aβと略す)が他のAβペプチドと一緒にミスフォールディングして凝集することによって引き起こされる有毒な凝集体と関連している。 これらのAβ凝集体は、アルツハイマー病の病理学的マーカーである老人斑(神経突起斑))に成長する。 これらの凝集体は不均一な性質を持っているため、X線結晶構造解析や核磁気共鳴(NMR)などの実験的手法では、その構造の特徴を明らかにすることが困難であった。 また、Aβ凝集体の原子シミュレーションは、その大きさと複雑さから、計算量が非常に多くなる。
Aβ凝集を防ぐことは、アルツハイマー病の治療薬を開発する上で有望な方法であると、NaeemとFaziliは文献調査で述べている。 2008年、Folding@homeは、数十秒単位の時間スケールでAβ凝集のダイナミクスを原子レベルで詳細にシミュレーションした。 これまでの研究では、約10マイクロ秒のシミュレーションしかできなかった。 Folding@homeは、これまでの研究よりも6桁長い時間スケールでAβのフォールディングをシミュレーションすることができた。 研究者たちは、この研究の結果を利用して、構造内の分子間相互作用の主な原因となるβヘアピンを特定した。 この研究は、パンデ研究室が将来の凝集研究のために、また凝集プロセスを安定化させる可能性のある小さなペプチドを見つけるための更なる研究のために準備をするのに役立った。
2008年12月、Folding@homeは、Aβ凝集体の毒性を阻害すると思われるいくつかの小さな薬物候補を発見した。 2010年には、タンパク質フォールディング機構センター(Center for Protein Folding Machinery)との緊密な協力のもと、これらの薬物候補の生体組織での試験が開始された。 2011年、Folding@homeは、Aβの凝集体形成を安定化させると思われるいくつかの変異のシミュレーションを完成させた。 これらの変異は、病気の治療薬の開発に役立つ可能性があり、Aβオリゴマーの核磁気共鳴分光法による実験的研究に大きく貢献している。 その年の後半、Folding@homeは、様々な天然酵素がAβの構造とフォールディングみにどのような影響を与えるかを決定するために、様々なAβフラグメントのシミュレーションを開始した。
ハンチントン病
ハンチントン病は、タンパク質の折り返しや凝集を伴う神経変性性遺伝性疾患である。 ハンチントンタンパク質のN末端にあるグルタミンアミノ酸の過剰な繰り返しが凝集を引き起こし、その挙動は完全には解明されていないが、本疾患に伴う認知機能の低下につながると考えられている。 他の凝集体と同様に、その構造を実験的に決定することは困難である。 科学者たちは、Folding@homeを用いて、ハンチントンタンパク質の凝集体の構造を研究し、凝集体がどのように形成されるかを予測し、凝集体の形成を止めるための合理的な医薬品設計法を支援している。 ハンチントンタンパク質のN17フラグメントは、この凝集を促進し、いくつかのメカニズムが提案されているが、このプロセスにおける正確な役割はほとんど不明である。 Folding@homeは、このフラグメントと他のフラグメントのシミュレーションを行い、疾患における役割を明らかにしてきた。2008年からは、アルツハイマー病の薬物設計法をハンチントン病に応用している。
がん(癌)
既知のがんの半分以上は、細胞周期を制御し、DNAが損傷した場合に細胞死のシグナルを出す、すべての細胞に存在するがん抑制タンパク質であるp53の突然変異が関与している。 p53の特定の変異は、これらの機能を破壊し、異常な細胞の成長を抑制せずに継続させ、結果として腫瘍を発生させる。 これらの突然変異の解析は、p53関連の癌の根本原因を説明するのに役立つ。 2004年には、Folding@homeを使用して、水の全原子シミュレーションにおけるp53のタンパク質二量体のリフォールディングの最初の分子動力学研究を行った。 このシミュレーションの結果は実験結果と一致し、以前は得られなかった二量体のリフォールディングについての洞察が得られた。 これは、分散型計算機プロジェクトによるがんに関する初の査読付き論文となった。 翌年、Folding@homeは、特定のタンパク質の安定性に重要なアミノ酸を特定する新しい方法を開発し、p53の変異の研究に使用した。 この方法は、がんを促進する突然変異を特定することに成功し、他の方法では実験的に測定することができなかった特定の突然変異の影響を決定することができた。
Folding@homeは、高分子クラウディングした化学的ストレスの多い環境下で、他のタンパク質のフォールディングを助けることで、細胞の生存に不可欠な役割を果たす熱ショックタンパク質であるタンパク質のシャペロンの研究にも使用されている。 急速に成長する癌細胞は特定のシャペロンに依存しており、いくつかのシャペロンは化学療法の抵抗性に重要な役割を果たしている。 これらの特定のシャペロンを阻害することは、効率的な化学療法薬の開発や、がんの広がりを抑えるための潜在的な作用機序と考えられている。 パンデ研究室では、Folding@homeを用いて、タンパク質フォールディング機構センター(Center for Protein Folding Machinery)と緊密に連携し、がん細胞に関与するこれらのシャペロンを阻害する薬剤を見つけたいと考えている。 また、研究者たちは、Folding@homeを使って、Srcキナーゼという酵素や、がんを含む多くの病気に関与している可能性のある大きなタンパク質であるエングレイルドホメオドメインの一部の形など、がんに関連する他の分子の研究にも取り組んでいる。 2011年、Folding@homeは、がん細胞表面受容体に結合することで、イメージングスキャンで癌腫を識別することができる小さなノッティンタンパク質EETIの動力学のシミュレーションを開始した。
インターロイキン2(IL-2)は、免疫系のT細胞が病原体や腫瘍を攻撃するのを助けるタンパク質である。 しかし、肺水腫などの重篤な副作用のため、がん治療薬としての使用は制限されている。 IL-2はT細胞とは異なる形で肺細胞に結合するため、この結合機構の違いを理解することが研究の課題となっている。 2012年には、Folding@homeは、免疫系の役割に300倍以上の効果がありながら、副作用が少ない変異型のIL-2の発見を支援した。 実験では、この変異型のIL-2は、腫瘍の成長を阻害するという点で、天然のIL-2よりも有意に優れていた。 製薬会社はこの変異体分子に関心を示しており、アメリカ国立衛生研究所は、治療薬としての開発を加速させるために、様々な腫瘍モデルを用いて試験を行っている。
不完全骨形成
骨形成不全症は、脆性骨疾患として知られており、致死的になる可能性のある不治の遺伝性骨疾患である。 この病気の人は、機能的な結合骨組織を作ることができない。 この疾患は、様々な構造的役割を果たし、哺乳類に最も多く存在するタンパク質であるI型コラーゲンの突然変異が最も一般的な原因となっている。 この突然変異は、コラーゲンの三重らせん構造の変形を引き起こし、自然に破壊されなければ、骨組織の異常や弱体化を引き起こす。 2005年、Folding@homeは、それまでのシミュレーション手法を改良した新しい量子力学的手法をテストした。 研究者は、Folding@homeをコラーゲンのフォールディングと折りたたみのミスフォールディングの研究に使用してきたが、アルツハイマー病やハンチントン病の研究と比較すると、この研究はパイロットプロジェクトとしての関心が高いようである。
ウイルス
Folding@homeは、インフルエンザやHIVなどの一部のウイルスが認識して生体細胞に侵入するのを防ぐ研究を支援している。 2011年、Folding@homeは、HIVの重要な構成要素である酵素RNase Hの動力学のシミュレーションを開始し、酵素を不活性化する薬の設計を試みた。 また、Folding@homeは、ウイルス感染と幅広い生物学的機能に不可欠なイベントである膜融合の研究にも利用されている。 この融合には、ウイルス融合タンパク質のコンフォメーション変化とタンパク質ドッキングが関与しているが、融合の背後にある正確な分子メカニズムはほとんどわかっていない。 融合現象は、数百マイクロ秒の間に50万個以上の原子が相互作用することもある。 このような複雑さから、一般的なコンピュータシミュレーションでは、数十ナノ秒の間に約1万個の原子が相互作用することになるが、これは数桁の違いある。 膜融合のメカニズムを予測するモデルの開発は、抗ウイルス薬を用いてこのプロセスを標的にする方法を科学的に理解するのに役立つだろう。 2006年には、マルコフ状態モデルとFolding@homeネットワークを応用して、融合の2つの経路を発見し、その他のメカニズムに関する知見を得た。
2007年、パンデ研究室は、小胞として知られる小細胞の詳細なシミュレーションをFolding@homeで行った後、融合中の構造変化のトポロジーを測定する新しい計算方法を導入した。 2009年には、研究者たちはFolding@homeを使って、ウイルスを宿主細胞にくっつけ、ウイルスの侵入を助けるタンパク質であるインフルエンザヘマグルチニンの変異を研究した。 ヘマグルチニンの変異は、ヘマグルチニンが宿主の細胞表面受容体分子にどの程度うまく結合するかに影響を与え、これによってウイルス株が宿主生物にどの程度感染するかが決定される。 ヘマグルチニンの変異の影響に関する知識は、抗ウイルス薬の開発に役立つ。 2012年現在、Folding@homeは、バージニア大学での実験研究を補完しながら、ヘマグルチニンのフォールディングと相互作用のシミュレーションを続けている。
2020年3月、Folding@homeは、治療法の発見やコロナウイルスのパンデミックについての詳細な研究を行っている世界中の研究者を支援するプログラムを開始した。 プロジェクトの第一段階では、SARS-CoV-2ウイルス、および関連するSARS-CoVウイルスからの薬剤化可能なタンパク質標的をシミュレートしているが、これらについては、利用可能なデータが大幅に増加している。
薬剤設計
薬物は、標的分子上の特定の位置に結合し、標的を無効にしたり、コンフォメーション変化を起こしたりするなど、所望の変化を引き起こすことで機能する。 理想的には、薬物は非常に特異的に作用し、他の生物学的機能を阻害することなく標的にのみ結合することが望ましい。 しかし、2つの分子がどこでどのように強固に結合するかを正確に決定することは困難である。 計算能力に限界があるため、現在のインシリコ(in silico)法は通常、正確さと速度を両立させなければならない。 例えば、計算コストのかかる自由エネルギー計算の代わりに、迅速なタンパク質ドッキングを使用するなどである。 Folding@homeの計算性能により、研究者は両方の方法を使用し、その効率性と信頼性を評価することができる。 コンピュータ支援創薬は、創薬のスピードアップとコスト削減につながる可能性がある。 2010年、Folding@homeは、MSMと自由エネルギー計算を用いて、X線結晶構造解析によって実験的に決定された結晶構造から、ヴィリンタンパク質のネイティブ状態を1.8オングストローム(Å)の二乗平均平方根誤差(RMSD)以内で予測した。 この精度は、本質的に構造化されていないタンパク質を含む、将来のタンパク質構造予測手法に意味を持つ。 科学者たちは、Folding@homeを利用して、最後の手段の薬であるバンコマイシンや、ペニシリンなどの抗生物質を分解するβ-ラクタマーゼを研究することで、薬剤耐性の研究を行ってきた。
化学活性は、タンパク質の活性部位に沿って発生する。 従来の薬物設計法では、標的タンパク質が1つの剛体構造に存在すると仮定して、この部位に強固に結合し、その活性を阻害する。 しかし、このアプローチが有効に働くのは、全タンパク質の約15%に過ぎない。 タンパク質にはアロステリックサイトが存在し、低分子と結合することでタンパク質の構造を変化させ、最終的にはタンパク質の活性に影響を与える。 これらの部位は魅力的な創薬標的であるが、その位置を特定するには非常に計算コストがかかる。 2012年には、Folding@homeとMSMを用いて、β-ラクタマーゼ、インターロイキン-2、RNase Hの3つの医学的に関連のあるタンパク質のアロステリックサイトを同定した。
既知の抗生物質の約半分は、細菌のリボソームの働きを阻害するもので、メッセンジャーRNAをタンパク質に翻訳することでタンパク質の生合成を行う、大きくて複雑な生化学的機械である。 マクロライド系抗生物質はリボソーム出口トンネルを塞ぎ、細菌の必須タンパク質の合成を妨げる。 2007年、パンデ研究室は、新しい抗生物質の研究と設計のための助成金を受けた。 2008年には、Folding@homeを使って、このトンネルの内部と、特定の分子がどのように影響するかを研究した。 リボソームの完全な構造は2011年の時点で決定されており、Folding@homeでは、リボソームタンパク質の機能の多くがほとんど解明されていないため、リボソームタンパク質のシミュレーションも行っている。
市民科学者による貢献
参加パターン
他の分散コンピューティングプロジェクトと同様に、Folding@homeはオンライン市民科学プロジェクトである。 こうしたプロジェクトでは、専門家ではない人々がコンピュータ処理能力を提供したり、プロの科学者が作成したデータの分析を手伝ったりする。 参加者はほとんど、あるいは明らかな報酬を受け取らない。
市民科学者の動機についての研究が行われてきたが、これらの研究のほとんどは、参加者が利他的な理由から参加する動機を持っていることを発見している。 つまり、科学者を助けたい、研究の発展に貢献したいと考えていることがわかった。 市民科学の参加者の多くは、研究のテーマに根底にある興味を持ち、自分の興味のある分野のプロジェクトへと引き寄せられていく。
Folding@homeもその点では変わりはなく、最近(2018)、400人以上の参加者を対象に行われた調査では、研究に貢献したいと考えていること、また、多くの参加者には、Folding@homeの科学者が調査している病気に罹患した友人や親戚がいることが明らかになった。
Folding@homeは、コンピュータハードウェアの愛好家(「オーバークロッカー」と呼ばれることもある)の参加者を集めている。 これらのグループは、プロジェクトにかなりの専門知識をもたらし、高度な処理能力を持つコンピュータを構築することができる。 他の分散コンピューティングプロジェクトでは、このようなタイプの参加者が集まり、プロジェクトは改造されたコンピュータの性能をベンチマークするために使用されることが多く、この趣味のこのような側面は、プロジェクトの競争的な性質によって対応されている。 個人やチームは、誰が最も多くのコンピュータ処理装置(CPU)を処理できるかを競うことができる。
このFolding@homeに関する最新の研究では、オンライングループのインタビューと民族誌的観察を行い、ハードウェア愛好家のチームが、処理出力を最大化するためのベストプラクティスを共有しながら一緒に作業することができることが示された。 このようなチームは、言語とオンライン文化を共有し、実践コミュニティになることができる。 このような参加パターンは、他の分散コンピューティングプロジェクトでも観察されている。
Folding@homeの参加者のもう一つの重要な観察点は、男性が多いことである。 これは他の分散型プロジェクトでも観察されている。 さらに、参加者の多くはコンピュータやテクノロジーを使った仕事やキャリアに従事している。
Folding@homeの参加者全員がハードウェアの愛好家というわけではない。 多くの参加者は、改造されていないマシンでプロジェクトのソフトウェアを実行し、競争的に参加している。 Folding@homeには10万人以上の参加者がいる。 しかし、参加者のうち、どの程度の割合がハードウェア愛好家なのかを把握することは困難である。 しかし、プロジェクト管理者によれば、処理能力の面では愛好家コミュニティの貢献度の方が大きいと語っている。
パフォーマンス

スーパーコンピュータのFLOPS性能は、従来のLINPACKベンチマークを実行することで評価される。 この短期的なテストでは、LINPACKがスーパーコンピュータのハードウェアに効率的にマップされるため、実世界のタスクでの持続的なパフォーマンスを正確に反映することは困難である。 コンピューティングシステムはアーキテクチャや設計が異なるため、直接比較することは困難である。 これにもかかわらず、FLOPSはスーパーコンピューティングで使用される主要な速度指標であることに変わりはない。 対照的に、Folding@homeは、ワークユニット(作業単位)が完了するのにかかる時間を測定することで、実経過時間を使用してFLOPSを決定する。
2007年9月16日、PlayStation 3の参加もあり、Folding@homeプロジェクトは、ネイティブ 1ペタFLOPS(参考: エクサスケール・コンピューティング)を超える持続的な性能を正式に達成し、あらゆる種類の計算機システムで初めての達成となった。 当時のTop500で最速のスパコンはBlueGene/Lで0.280ペタFLOPSであった。 翌年の2008年5月7日にはネイティブ 2ペタFLOPSを超える持続性能を達成し、2008年8月にはネイティブ 3ペタFLOPS、2008年9月28日にはネイティブ 4ペタFLOPSのマイルストーンを達成した。 2009年2月18日には、Folding@home がネイティブペタFLOPS 5ペタFLOPSを達成し、この5つのレベルを達成した最初の計算機プロジェクトとなった。 これに対して、2008年11月の最速スーパーコンピュータはIBMのRoadrunnerで1.105ペタFLOPSであった。 2011年11月10日のFolding@homeの性能は、6ネイティブペタFLOPSを超え、これはx86の8ペタFLOPS近くに相当する。2013年5月中旬には、Folding@homeは7ネイティブペタFLOPSを超え、14.87 x86ペタFLOPSに相当する。その後、6月21日には8ネイティブペタFLOPSを達成し、同年9月9日には9ネイティブペタFLOPSを達成、17.9 x86 ペタFLOPSを達成した。2016年5月11日、Folding@homeは100 x86 ペタFLOPSの達成に向けて動き出したと発表した。
2020年のコロナウイルスパンデミックによる意識の高まりと、市民科学者のプロジェクトへの参加から、さらなる利用が拡大した。 2020年3月20日、Folding@homeはTwitterを通じて、470ネイティブペタFLOPS以上で稼働していることを発表した(958 x86ペタFLOPSに相当)。 同年3月25日までに768ペタFLOPS、つまり1.5 x86エクサFLOPSに達し、初のエクサFLOPコンピューティングシステムとなった。
ポイント
他の分散コンピューティングプロジェクトと同様に、Folding@home は、クレジットシステムを通じてプロジェクトへのユーザのコンピューティング貢献度を定量的に評価する。 ポイントは、プロジェクトがリリースされる前に、そのプロジェクトからの1つ以上のワークユニット(作業単位)を公式のリファレンスマシン上でベンチマークすることによって決定される。 各ユーザは、すべてのワークユニットを完成させた場合にこれらの基本ポイントを受け取ることができるが、秘密のパスキーを登録することで、計算の難易度が高いユニットや科学的な優先順位が高いユニットを確実かつ迅速に完成させた場合には、ワークユニットの成功率が80%を超えることや、10個以上の有効なワークユニットを送信するなどの条件付きでボーナスポイントを追加で受け取ることができる。 また、ユーザは複数のマシン上のクライアントからの作業に対してもクレジットを受け取ることができる。 このポイントシステムは、与えられたクレジットと科学的結果の価値を一致させる試みである。
ユーザは自分の貢献をチームに対して登録することができ、メンバー全員のポイントを合算することができる。 ユーザは自分のチームを立ち上げることも、既存のチームに参加することもできる。 場合によっては、チームは、インターネットフォーラムのようなコミュニティ主導のヘルプや勧誘の情報源を持つこともある。 ポイントは、プロジェクトのために最も多くの計算をするために、個人とチームの間で友好的な競争を促進することができ、フォールディングコミュニティに利益をもたらし、科学研究を加速させることができる。 個人とチームの統計は、Folding@home のウェブサイトに掲載される。
ユーザが新しいチームを結成しなかったり、既存のチームに参加しなかったりすると、そのユーザは自動的に「デフォルト」チームのメンバーになる。 この「デフォルト」チームのチーム番号は「0」で、統計情報は、この「デフォルト」チームとして特別に命名されたチームのために蓄積される。
ソフトウェア
ユーザー側のFolding@homeソフトウェアは、ワークユニット、コア、クライアントという3つの主要なコンポーネントから構成されている。
ワークユニット
ワークユニット(Work units, 作業単位)とは、クライアントに処理を依頼するタンパク質データのことである。 作業単位は、マルコフモデルにおける状態間のシミュレーションの断片である。 ワークユニットがダウンロードされ、ボランティアのコンピュータで完全に処理された後、それはFolding@homeのサーバーに戻され、ボランティアにクレジットポイントが与えられる。 このサイクルは自動的に繰り返される。 すべてのワークユニットには期限があり、この期限を超えた場合、ユーザーはクレジットを取得できず、自動的に別の参加者に再発行される。 タンパク質のフォールディングは連続的に行われ、多くのワークユニットは前任者から生成されるため、妥当な期間が経過してもワークユニットが返却されない場合は、シミュレーションプロセス全体が正常に進行するようになっている。 これらの期限の関係上、Folding@homeの最小システム要件は、Pentium 3 450 MHz CPUとStreaming SIMD Extensions(SSE)である。 しかし、高性能クライアント用のワークユニットは、単一プロセッサクライアント用のワークユニットよりもはるかに短い期限が設定されており、それは科学的利益の大部分がシミュレーションを迅速に完了することに依存しているためである。
一般公開前に、ワークユニットはいくつかの品質保証段階を経て、問題のあるものが完全に利用可能にならないようにする。 これらのテスト段階には、Folding@home全体での最終的な完全リリースの前に、内部テスト、ベータテスト、および高度テストが含まれる。 Folding@homeのワークユニットは、処理中にまれにエラーが発生する場合を除き、通常、一度だけ処理される。 もしこれが3人の異なるユーザに発生した場合、そのユニットは自動的に配布から除去される。 Folding@homeサポートフォーラムは、問題のあるハードウェアに起因する問題と不良のワークユニットに起因する問題を区別するために使用することができる。
コア
「FahCores(ファーコア)」と呼ばれ、しばしば「Core(コア)」と略される特殊な分子動力学プログラムは、バックグラウンドプロセスとしてワークユニット上で計算を実行する。 Folding@homeのコアの大部分は、手動で最適化されたアセンブリ言語コードとハードウェアの最適化からなる、最も高速で最も一般的な分子動力学ソフトウェアパッケージの一つであるGROMACSをベースにしている。 GROMACSはオープンソースのソフトウェアで、パンデ研究室とGROMACSの開発者とは協力関係を持っているが、Folding@homeではデータの妥当性を確保するためにクローズドソースのライセンスを使用している(すなわちソースコードを公開していない)。 あまりアクティブではないコアには、ProtoMol(新しいアルゴリズムのテストに向く)とSHARPENがある。 かつてFolding@homeはAMBER、CPMD、Desmond、TINKERを使用してきたが、これらのコアは引退しており、現役ではなくなっている。 これらのコアの中には、周囲の溶媒(通常は水)を原子単位でモデル化する明示的な溶媒和計算を行うものもあれば、溶媒を数学的連続体として扱う暗黙の溶媒和計算を行うものもある。 コアはクライアントから分離されており、クライアントの更新を必要とせずに科学的手法を自動的に更新できるようになっている。 コアは定期的にアプリケーション・チェックポインティングを作成し、中断されても起動時にその時点から作業を再開できるようにしている。
クライアント
Folding@homeの参加者は、パーソナルコンピュータにクライアントプログラムをインストールする。 ユーザは、バックグラウンドで他のソフトウェアコンポーネントを管理するクライアントと対話する。 ユーザはクライアントを通じて、折り畳み処理を一時停止したり、イベントログを開いたり、作業の進捗状況を確認したり、個人の統計情報を表示したりすることができる。 コンピュータ・クライアントは、通常のコンピュータの使用に影響を与えないように、非常に低い優先度でバックグラウンドで継続的に実行され、アイドル処理能力を使用する。 CPUの最大使用量は、クライアントの設定で調整できる。 クライアントは、Folding@homeサーバに接続し、ワークユニットを取得し、クライアントの設定、オペレーティングシステム、および基礎となるハードウェアアーキテクチャに適したコアをダウンロードすることができる。 処理後、ワークユニットは、Folding@homeサーバに戻される。 コンピュータ・クライアントは、ユニプロセッサ・システムやマルチコア・プロセッサ・システム、グラフィックス・プロセッシング・ユニットに合わせて調整されている。 各ハードウェアアーキテクチャの多様性と処理性能により、Folding@homeは、多くの種類のシミュレーションをタイムリーに(数年ではなく数週間から数ヶ月で)効率的に完了させることができ、これは科学的価値の高いものである。 これらのクライアントを組み合わせることで、研究者は、これまで計算で取り組むことが非現実的と考えられていた生物医学的な問題を研究することが可能になる。
プロのソフトウェア開発者は、クライアント側とサーバー側の両方で、Folding@homeのコードの大部分を担当している。 開発チームには、Nvidia、ATI、Sony、Cauldron Developmentのプログラマーが含まれている。 クライアントは、Folding@homeの公式ウェブサイトまたはその商用パートナーからのみダウンロードすることができ、Folding@homeのコンピュータファイルとのみやりとりする。 クライアントは、Folding@homeのデータサーバー(ポート8080、代替として80を使用)にデータをアップロードしたりダウンロードしたりし、通信は2048ビットのデジタル署名を使用して検証される。 クライアントのグラフィカル・ユーザー・インターフェース(GUI)はオープンソースであるが、クライアントはセキュリティと科学的整合性を理由にプロプライエタリなソフトウェアである。
しかし、プロプライエタリなソフトウェアを使用することのこの合理性は、ライセンスは遡及的に法的な領域で強制力を持つことができるかもしれないが、実行可能なバイナリファイルの改変(パッチ適用としても知られる)を実質的に防ぐことができないため、議論の余地がある。 同様に、バイナリのみの配布では、インターネット経由でダウンロードされている間の中間者攻撃や、第三者によるバイナリの再配布によって、バイナリ状態のまま(つまりパッチを当てられたまま)、あるいは変更後のバイナリを逆コンパイルして再コンパイルすることによって、実行バイナリコードの悪意のある変更を防ぐことができない。 このような変更は、バイナリファイルとトランスポートチャネルが署名されていて、受信者やシステムがデジタル署名を検証できる場合には可能であるが、必ずしもそうとは限らない。 いずれにしても、Folding@home の場合、クライアント・ソフトウェアによって処理される入力データと出力結果の両方がデジタル署名されているので、作業の完全性は、クライアント・ソフトウェア自体の完全性から独立して検証することができる。
Folding@homeでは、ネットワークのためにCosmソフトウェアライブラリを使用している。 Folding@homeは2000年10月1日に立ち上げられ、生体分子システムを対象とした最初の分散コンピューティングプロジェクトであった。 最初のクライアントはスクリーンセーバーで、コンピュータが使用されていないときに実行された。 2004年には、パンデ研究室はデビッド・P・アンダーソンと共同で、オープンソースのBOINCフレームワーク上で補助的なクライアントをテストした。 このクライアントは2005年4月にクローズドベータ版としてリリースされたが、この方法は実行不可能となり、2006年6月に棚上げされた。
グラフィックス・プロセッシング・ユニット
グラフィックス・プロセッシング・ユニット(Graphics Processing Units = GPU)の特殊なハードウェアは、ビデオゲームなどの3Dグラフィックス・アプリケーションのレンダリングを高速化するように設計されており、ある種の計算ではCPUを大幅に上回る性能を発揮する。 GPUは、最も強力で急速に成長しているコンピューティングプラットフォームの1つであり、多くの科学者や研究者は、グラフィックス・プロセッシング・ユニット上での汎用コンピューティング(GPGPU)を追求している。 しかし、GPUハードウェアは、グラフィックス以外のタスクに使用するのは難しく、通常、大幅なアルゴリズムの再構築と、基礎となるアーキテクチャの高度な理解を必要とする。 このようなカスタマイズは、ソフトウェア開発リソースが限られている研究者にとってはなおさら困難である。
Folding@homeでは、オープンソースのOpenMMライブラリを使用している。 このライブラリは、2つのアプリケーション・プログラミング・インターフェース(API)レベルを持つブリッジ設計パターンを使用して、分子シミュレーション・ソフトウェアの基礎となるハードウェア・アーキテクチャにインターフェースする。 OpenMMベースのGPUシミュレーションでは、ハードウェアの最適化が追加されたことで、大幅な変更は必要とせず、手作業でチューニングされたGPUコードとほぼ同等の性能を実現し、CPUの実装を大幅に上回る性能を発揮する。
2010年以前は、GPGPUコンシューマーグレードのハードウェアの計算信頼性はほとんど知られておらず、GPUメモリに内蔵された誤り検出と訂正がないことに関する状況証拠により、信頼性の懸念が生じた。 2010年、Folding@home ネットワーク上の2万台以上のホストを対象とした大規模なGPU科学的精度テストでは、テストされたGPUの3分の2のメモリサブシステムでソフトエラーが検出された。 これらのエラーはボードアーキテクチャと強く相関しているが、ソフトウェア側のエラー検出などのハードウェアの特性に注意を払っている限り、信頼性の高いGPUコンピューティングは大いに実現可能であると結論づけている。
Folding@homeの第一世代のGPUクライアント(GPU1)が2006年10月2日に公開され、CPUベースのGROMACSと比較して、いくつかの計算で20~30倍の高速化を実現した。 これは、GPUが分散コンピューティングや主要な分子動力学計算に使用された初めての試みであった。 GPU1は研究者にGPGPUソフトウェアの開発に関する重要な知識と経験を与えたが、2008年4月10日にDirectXの科学的な不正確さに対応して、第2世代のクライアントであるGPU2に引き継がれた。 GPU2の導入後、GPU1は6月6日に正式に引退した。 GPU1に比べて、GPU2はより科学的な信頼性と生産性が高く、ATIやCUDA対応のNvidia GPU上で動作し、より高度なアルゴリズム、より大きなタンパク質、タンパク質シミュレーションのリアルタイム可視化をサポートしていた。 これに続き、2010年5月25日には第3世代のFolding@homeのGPUクライアント(GPU3)がリリースされた。 GPU3は、GPU2との後方互換性を持ちながらも、より安定性、効率性、柔軟性に優れた科学的能力を持ち、OpenCLフレームワークの上にOpenMMを使用していた。 これらのGPU3クライアントはオペレーティングシステムLinuxとmacOSをネイティブにはサポートしていなかったが、Nvidiaのグラフィックカードを搭載したLinuxユーザーはWineソフトウェアアプリケーションを介してGPU3を実行することができた。 GPUは、Folding@homeのFLOPSの中で最も強力なプラットフォームであることに変わりはない。 2012年11月現在、GPUクライアントは、プロジェクト全体のx86 FLOPSスループットの87%を占めている。
LinuxでのNvidiaとAMDのグラフィックスカードのネイティブサポートは、CUDAではなくOpenCLを使用するFahCore 17で導入された。
PlayStation 3
2007年3月から2012年11月まで、Folding@homeはPlayStation 3の計算能力を利用していた。 その開始時において、メインのストリーミングCellプロセッサ(Cell Broadband Engine)は、いくつかの計算でPCの20倍の速度を実現し、Xbox 360のような他のシステムにはない処理能力を発揮していた。 PS3 の高速性と効率性は、アムダールの法則に基づいて最適化する価値のある他の機会をもたらし、計算効率と全体的な精度の間のトレードオフを大きく変え、より複雑な分子モデルをわずかな計算コストで使用できるようにした。 これにより Folding@homeは、他の方法では計算上不可能であった生物医学的な計算を実行できた。
PS3クライアントは、ソニーとパンデ研究室の共同開発により開発され、2007年3月23日にスタンドアロンのクライアントとしてリリースされた。 このリリースにより、「Folding@home」は、PS3を利用した初めての分散コンピューティングプロジェクトとなった。 翌年2月5日にはプロジェクト参加者が100万人を突破、9月18日には、PS3クライアントが「Life with PlayStation」のチャネルに登場、11月6日にはグッドデザイン賞金賞を受賞した。導入当時は、計算の種類で言えば、CPUの柔軟性とGPUの高速性の中間に位置していた。 ただし、パソコン上で動作するクライアントとは異なり、「Folding@home」を起動したPS3では他の操作を行うことができなかった。 PS3の統一されたコンソール環境は、テクニカルサポートを容易にし、「Folding@home」をより使いやすくした。 また、PS3にはGPUへのデータストリーミング機能があり、現在のタンパク質の動力学を原子レベルでリアルタイムに可視化するために使用されていた。
ソニーは、2012年11月6日、「Life with PlayStation」で提供しているPS3クライアント「Folding@home」およびその他のサービスのサポートを終了した。 Folding@home」は、5年7ヶ月間で1,500万人以上のユーザーが1億時間以上の計算量を提供し、病気の研究に大きく貢献してきた。 パンデ研究室との話し合いの結果、ソニーはこのプロジェクトを終了することを決定した。 パンデ氏は、PlayStation 3のクライアントを、このプロジェクトにとって「ゲームチェンジャー」だと考えていた。
マルチコア処理クライアント
Folding@homeは、最新のマルチコア・プロセッサの並列計算能力を利用することができ、複数のCPUコアを同時に使用することで、シミュレーション全体をはるかに早く完了させることができる。 同じ時間でより長いシミュレーション軌道を実行し、また大規模なシミュレーションを多くの別々のプロセッサに分散するという従来の困難を軽減するために、この方法は科学的にも価値のある方法である。 Journal of Molecular Biology誌に掲載された2007年の論文では、マルチコア処理に依存することで、実験的なフォールディングと一致したビリン・タンパク質の一部のフォールディングを、シングルプロセッサクライアントで可能なものよりも約10倍長くシミュレーションしたと報告された。
2006年11月、第一世代の対称型マルチプロセシング(SMP)クライアントがオープンベータテスト用に公開され、これはSMP1と呼ばれた。 このクライアントは、並列処理にMessage Passing Interface(MPI)通信プロトコルを使用していたが、当時のGROMACSコアは複数スレッドでの使用を想定していなかった。 分散コンピューティングプロジェクトでMPIを使用した初めての試みであった。 クライアントはLinuxやmacOSなどのUnixベースのOSでは問題なく動作したものの、Windowsでは問題があった。 2010年1月24日、SMPクライアントの第二世代であり、SMP1の後継となるSMP2がオープンベータとしてリリースされ、複雑なMPIは、より信頼性の高いスレッドベースの実装に置き換えられた。
SMP2は、異常に大きく、計算集約的で、科学的優先度が非常に高いタンパク質をシミュレートするように設計された、Big Advanced(bigadvまたはBAとも)ワークユニットの特別なカテゴリのトライアルをサポートしていた。 これらのユニットは、もともと最低8個のCPUコアを必要としていたが、2012年2月7日に16個のCPUコアに引き上げられた。 標準的なSMP2ワークユニットよりもハードウェア要件が増えたことに加えて、ランダム・アクセス・メモリ(RAM)やインターネットの帯域幅などのシステムリソースが必要となった。 その見返りとして、これらを実行するユーザは、SMP2のボーナスポイントシステム以上の20%高い報酬が与えられた。 bigadvカテゴリでは、以前はスーパーコンピュータのクラスタを使用しなければならず、Folding@home上では他のどこでも実行できなかったような、特に要求の厳しいシミュレーションを長時間実行することができた。 ところが、bigadvユニットを実行できるハードウェアを持っている多くのユーザは、後からCPUコアの最小値が増加した時に、そのハードウェアがbigadvワークユニットには不適格とみなされ、通常のSMPワークユニットしか実行できなくなってしまった。 このことはプログラムに多額の資金を投資した多くのユーザーをいら立たせ、bigadvの目的でハードウェアが使用できなくなってしまった。 その結果、パンデは2014年1月にbigadvプログラムを2015年1月31日に終了することを発表した。
V7クライアント

V7クライアントは、Folding@homeクライアントソフトの第7世代となる最新版で、Windows、macOS、Linux OS用の以前のクライアントを全面的に書き換え、統一化したものである。 2012年3月22日にリリースされたV7は、以前のクライアントと同様に、バックグラウンドでFolding@homeを非常に低い優先度で動作させることができ、他のアプリケーションが必要に応じてCPUリソースを使用できるようになっている。 それは、インストール、起動、操作が初心者にとってよりユーザーフレンドリーになるように設計されており、以前のクライアントよりも研究者に科学的な柔軟性を提供している。 V7では、Tracを使用してバグチケットを管理し、ユーザが開発プロセスを見てフィードバックを提供できるようにしている。
V7は、マルチコアに対応した1個のCPUスロットと、対応GPUごとにGPUスロットを設け、複数のCPUコアを利用するように設計された。
V7は、4つの統合された要素から構成されている。 ユーザは通常、FAHControlと名付けられたV7のオープンソースGUIを使用して操作する。 これには、初心者向け、上級者向け、およびエキスパート向けのユーザ・インタフェースモードがあり、1台のコンピュータから多数のリモート・フォールディング・クライアントを監視、設定、および制御する機能を備えている。 FAHControlは、各FAHSlot(単にスロットと呼ばれる)を管理するFAHClientというバックエンドアプリケーションに対して指示をする。 各スロットは、単独でワークユニットのダウンロード、シミュレーション処理、その結果のアップロードを行うことができる。 かつては別個であった、Folding@home V6ユニプロセッサ版、SMP版、GPUコンピュータクライアントの代わりとして機能する。 そしてPS3のビューアを模したFAHViewerは、現在処理中のタンパク質のリアルタイム3Dレンダリングを表示する。
Google Chrome
2014年には、Google ChromeとChromiumのWebブラウザ用のクライアントがリリースされ、ユーザがFolding@homeをWebブラウザで実行できるようになった。 このクライアントでは、ChromiumベースのWebブラウザに搭載されているGoogle Native Client(NaCl)機能を利用して、ユーザーのマシン上のサンドボックスでFolding@homeのコードをネイティブに近い速度で実行していた。 NaClの段階的な廃止とFolding@homeでの変更により、Webクライアントは2019年6月に恒久的にシャットダウンされた。
Android
2015年7月、Android 4.4 KitKat以降を搭載した端末を対象としたAndroid携帯電話向けのクライアントがGoogle Playで公開された。 その後、2018年2月16日、ソニーと共同で提供していたAndroidクライアントがGoogle Playから削除された。将来的にはオープンソースの代替版を提供する計画が発表された。
他の分子シミュレータとの比較
Rosetta@home
Rosetta@homeは、タンパク質の構造予測を目的とした分散コンピューティングプロジェクトであり、最も正確な三次構造予測の一つである。 Rosettaのソフトウェアから得られる立体配座状態を利用して、Folding@homeシミュレーションの出発点としてマルコフ状態モデルの初期化に利用することができる。 逆に、(Rosettaの)構造予測アルゴリズムは、熱力学的モデルと運動論的モデル、およびタンパク質フォールディングシミュレーションのサンプリングの側面から改善することができる。 Rosettaは最終的なフォールディング状態を予測するだけで、どのようにフォールディングが進行するかを予測するものではないため、Rosetta@homeとFolding@homeは補完的なものであり、全く異なる分子問題に対応する。
Anton
Antonは分子動力学シミュレーションのために構築された専用のスーパーコンピュータである。 2011年10月の時点で、AntonとFolding@homeは2つの最も強力な分子動力学システムであった。 Antonは、2010年にミリ秒領域に達した単一の分子軌道のように、非常に計算コストのかかる単一の(長い)分子軌道を生成する能力においてユニークであった。 このような長い軌跡は、いくつかのタイプの生化学的問題に特に役立つ。 しかし、Antonは解析にマルコフ状態モデル(MSM)を使用していない。 2011年、パンデ研究室は、2つの100µsのAntonシミュレーションからMSMを構築し、Antonの従来の解析では見えなかった代替のフォールディング経路を発見した。 その結果、限られた数の長い軌道から構築されたMSMと、多くの短い軌道から構築されたMSMの間には、ほとんど違いがないと結論づけた。 2011年6月、Folding@homeは、Antonと比較した手法をより適切に判断するために、Antonシミュレーションのサンプリングを追加した。 ただし、Folding@homeの短い軌道が分散コンピューティングや他の並列化手法に適しているのとは異なり、長い軌道はタンパク質の位相空間を十分にサンプリングするために適応的サンプリングを必要としない。 このため、Antonのシミュレーション手法とFolding@homeのシミュレーション手法を組み合わせることで、この空間のより完全なサンプリングが可能になる可能性がある。
歴史
- 2000年10月1日、プロジェクトを開始。
- 2007年3月22日、PlayStation 3(PS3)に対応。3日後には700T(テラ)FLOPS以上の演算能力を獲得し、従来1年以上かかっていた複雑なシミュレーションが数週間で完了した。
- 2007年9月16日、分散コンピューティング史上初となる1P(ペタ)FLOPSに到達(1秒間に1000兆回の演算能力)。
- 2007年9月24日、PS3クライアントのみの合計で当時のスーパーコンピュータの能力に匹敵する1PFLOPSに到達。
- 2007年11月1日、世界一強力な分散コンピューティングネットワークとしてギネス世界記録に認定。
- 2008年11月9日現在、計4.247PFLOPS、うちGPUの処理能力は2.226PFLOPS、PS3による処理能力は1.733PFLOPS。
- 2012年3月23日現在、計5.427PFLOPS。
- 2012年10月22日、PS3クライアントの終了を発表(2012年11月6日終了、延べ1500万人のユーザーが参加した)。
- 2015年1月13日、Android 4.4以上搭載のスマートフォン/タブレット向けクライアントアプリをリリース。当初はXperiaシリーズのみ対応、のち条件を満たす他機種にも対応。
- 2016年1月6日現在、計80.79PFLOPS、うちGPUの処理能力は78PFLOPS(96%)。GPUはNVIDIAのFermiが8割を占める。
- 2020年2月27日、新型コロナウイルス感染症(COVID-19)に対する取り組みを発表。
- 2020年3月25日、分散コンピューティング史上初となる1E(エクサ)FLOPS(1秒間に100京回の演算能力)に到達。
- 2020年4月、2.4EFLOPS(毎秒240京回)到達。これは世界のTOP500の合計を上回る能力。
脚注
注釈
関連項目
- BOINC
- タンパク質構造予測
- タンパク質フォールディング
- タンパク質間相互作用
- Foldit
- グリッド・コンピューティング
- 分散コンピューティング
- 市民科学
- GPUを用いた分子モデリング
- SETI@home
- World Community Grid
- DreamLab
外部リンク
- 公式ウェブサイト
- Folding@home (@foldingathome) - Twitter
- 『Folding@home』 - コトバンク