エンパグリフロジン
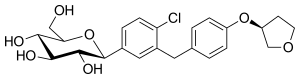
| |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | ジャディアンス |
| Drugs.com | entry |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 投与方法 | 経口 |
| 識別 | |
|
CAS番号 |
864070-44-0 |
| ATCコード | A10BX12 (WHO) |
| PubChem | CID: 11949646 |
| UNII | HDC1R2M35U |
| KEGG |
D10459 |
| 化学的データ | |
| 化学式 | C23H27ClO7 |
| 分子量 | 450.91 g/mol |
| |
| |
エンパグリフロジン(Empagliflozin)は、ナトリウム・グルコース共輸送体(SGLT)-2 阻害作用を有する糖尿病治療薬である。グルコースは通常、腎臓の糸球体で一旦原尿中に排出され、尿細管から再吸収される。SGLT-2は腎臓の近位尿細管に発現していて、グルコースの再吸収の約90%を担っているとされる。血糖値が過剰に高い場合、SGLT-2を阻害することにより、尿中へ排泄されるグルコースが増加し、血液中のグルコース濃度が適正化される。商品名ジャディアンス。開発コードBI-10773。
承認
米国および欧州で2013年5月、日本で2013年10月に承認申請され、欧州で2014年5月、米国で2014年8月、日本で2014年12月に承認された。
副作用
重大な副作用として添付文書に記載されているものは、低血糖(他剤、特にSU薬との併用)(2.3%)、脱水(0.1%)、ケトアシドーシス、腎盂腎炎、敗血症である。
10mgおよび25mgの用量で、泌尿器系器官の感染症の頻度が増加することが報告されている。尿量の増加および体重の減少をきたす症例が多いことが報告されている。
選択性
ナトリウム・グルコース共輸送体(SGLT)には、少なくとも6種類の遺伝子産物が含まれている。それらのうち、SGLT-1は小腸・腎臓・心筋・骨格筋・脳などの細胞膜に発現していると云われており、小腸粘膜に多く発現するSGLT-1は、食物由来のグルコースの吸収に関与している。小腸粘膜においてSGLT-1機能が阻害されると、グルコースとガラクトースの吸収不良を生じる可能性があり、下痢と脱水をきたすおそれがある。ゆえに糖尿病治療に用いるSGLT-2阻害薬は、高い選択性すなわちSGLT-1を高濃度においてのみ阻害するような性質が必要であると考えられる。また、上述の通りSGLT-2は腎臓の近位尿細管細胞に多く発現している。
エンパグリフロジンのSGLT-1に対するIC50は8,300nMであり、SGLT-2に対するIC50は3.1nMである。また有色ラットに14C-エンパグリフロジンを5mg/kg経口投与したときの組織中放射能濃度を定量的全身オートラジオグラフィーにより測定したところ、投与1時間後(Cmax:447ng Eq/g)での組織中濃度は小腸339ng Eq/g、腎臓2,540ng Eq/g、心筋(データ無し)、骨格筋(データ無し)、脳0ng Eq/g(移行無し)であった。
効能・効果
- 2型糖尿病
- HFpEF - 2019年10月現在、日本を含む国際共同P3試験「EMPEROR HF-Preserved」を行っていて、予定患者数約4100人、主要評価項目は「心血管死または心不全による入院の最初の事象までの時間(最大38カ月)」で、2020年終了予定。
エビデンス
大規模臨床試験であるEMPA-REG OUTCOME(患者数:7,020名、中央観察期間:3.1年)において、心血管死亡(ハザード比:0.62)、総死亡(ハザード比:0.68)、心不全による入院(ハザード比:0.65)のいずれも偽薬群に対してエンパグリフロジン群(10mgまたは25mg)で有意な減少が認められた。一次評価項目は「心血管死亡+非致死性心筋梗塞+非致死性脳卒中」でハザード比は0.86(優越性検定:p = 0.04)、主要二次評価項目は「一次評価項目+不安定狭心症による入院」でハザード比は0.89(優越性検定:p = 0.08)であった。
