プロスタサイクリン

| |
| |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 薬物動態データ | |
| 半減期 | 42 seconds |
| 識別 | |
|
CAS番号 |
35121-78-9 |
| PubChem | CID: 5282411 |
| IUPHAR/BPS | 1915 |
| ChemSpider |
102770 |
| UNII |
DCR9Z582X0 |
| KEGG | D00106 |
| ChEMBL |
CHEMBL1139 |
| 化学的データ | |
| 化学式 | C20H32O5 |
| 分子量 | 352.47 g·mol−1 |
| |
プロスタサイクリン(Prostacyclin)またはプロスタグランジンI2(Prostaglandin I2、PGI2)は、エイコサノイド系の脂質分子であるプロスタグランジンの一種である。血小板の活性化抑制作用と、血管拡張作用がある。
機能
プロスタサイクリン(PGI2)は、主に一次止血(血栓形成の一部)に関与する血小板の栓形成を防ぐ。これは、血小板の活性化を阻害することによって行われる。また、血管拡張剤としても有効である。プロスタサイクリンの相互作用は、同じくエイコサノイドであるトロンボキサン(TXA2)の相互作用とは対照的である。これらのことは、血管障害に関連したこの2つの生理活性物質による心血管恒常性維持のメカニズムを強く示唆している。
作用機序
プロスタサイクリンの効果 機序 反応 古典的機能 血管平滑筋 緊張
↑cAMP, ↓ET-1
↓Ca2+, ↑K+↓SMC増殖
↑血管拡張抗増殖性 ↑cAMP
↑PPARγ↓線維芽細胞増殖
↑アポトーシス抗血栓性 ↓TXA2
↓PDGF↓血小板凝集
↓血小板の血管壁への付着新規機能 抗炎症 ↓IL-1, IL-6
↑IL-10↓炎症性サイトカイン
↑抗炎症性サイトカイン抗原性 ↓VEGF
↓TGF-β↓血管新生
↑ECMリモデリング
前述のように、プロスタサイクリン(PGI2)は健康な内皮細胞から放出され、近傍の血小板や内皮細胞のGタンパク質共役受容体が関与するパラクリンシグナルカスケードによってその機能を発揮する。血小板のGsタンパク質共役受容体(プロスタサイクリン受容体)は、PGI2と結合すると活性化される。cAMPは、血小板の過度の活性化を抑制し(血液循環を促進)、トロンボキサンA2(TXA2)の結合による細胞質カルシウム濃度の上昇(血小板の活性化とそれに続く凝固を引き起こす)を打ち消す働きをする。PGI2は、内皮のプロスタサイクリン受容体にも結合し、同様に細胞質内のcAMP濃度を上昇させる。このcAMPは、プロテインキナーゼA(PKA)を活性化する。そして、PKAはミオシン軽鎖キナーゼのリン酸化を促進してカスケードを継続し、それを阻害し、平滑筋の弛緩と血管拡張をもたらす。なお、PGI2とTXA2は生理的アンタゴニストとして働く。
薬理学
プロスタサイクリンの産生は、NSAIDがシクロオキシゲナーゼ酵素COX1およびCOX2に作用することで阻害される。これらの酵素はアラキドン酸をプロスタサイクリンの直接の前駆体であるプロスタグランジンH2(PGH2)に変換する。トロンボキサン(血小板凝集を促進するエイコサノイド)もCOX酵素の下流にあるので、NSAIDの効果はバランスをとるように作用すると思われるかも知れない。しかし、プロスタサイクリン濃度はトロンボキサン濃度よりもはるかに早く回復するため、アスピリン投与では最初はほとんど効果がないが、最終的には血小板凝集を防ぐことができる(プロスタグランジンが再生産されるため、プロスタグランジンの効果が優勢になる)。このことは、TXA2とPGI2というそれぞれの分子を産生する細胞を理解することで説明できる。PGI2は主に有核の内皮細胞で産生されるため、NSAIDによるCOX阻害は、COX遺伝子の活性化が進み、その後、PGI2の生成を触媒するCOX酵素が多く産生されることで、時間の経過と共に克服される。一方、TXA2は主に無核血小板から放出される。無核血小板は、NSAIDによるCOX阻害に対応してCOX遺伝子の転写を増やすことができない。なぜなら、そのような作業を行うのに必要なDNA材料がないからである。このため、NSAIDは血液循環を促進し、血栓症を抑制するPGI2を優位に作用させることができる。
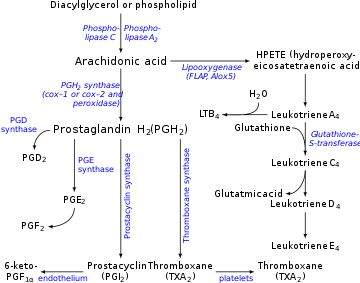
生合成
プロスタサイクリンは、動脈や静脈の壁を覆う内皮細胞において、プロスタサイクリン合成酵素の作用により、プロスタグランジンH2(PGH2)から産生される。プロスタサイクリンは独立したメディエーターと考えられているが、エイコサノイドの命名法ではPGI2(プロスタグランジンI2)と呼ばれ、プロスタグランジン、トロンボキサンとともにプロスタノイドの仲間である。PGI2は、ヒトでは主にCOX2に由来し、血管内皮から放出される主要なアラキドン酸代謝物である。この点については議論があり、血管内皮細胞の主要なプロスタサイクリン産生シクロオキシゲナーゼをCOX1とする意見もある。
3系統のプロスタグランジンPGH3もプロスタサイクリン合成酵素の経路をたどり、別のプロスタサイクリンであるPGI3が生成される。非限定的な用語「プロスタサイクリン」は、通常、PGI2を指す。PGI2は、ω-6アラキドン酸に由来する。PGI3は、ω-3エイコサペンタエン酸に由来する。
歴史
1960年代、ジョン・ベーンら英国の研究チームは、アナフィラキシーや呼吸器疾患におけるプロスタグランジンの役割について研究を始めた。ベーンは、王立外科医師会のチームと共同で、アスピリン等の経口抗炎症薬がプロスタグランジンの合成を阻害することを発見した。この重要な発見により、体内でのプロスタグランジンの役割をより深く理解できるようになった。
ウエルカム財団のサルバドール・モンカダ率いるチームは、血小板の凝集を抑制する「PG-X」と呼ばれる脂質メディエーターを発見していた。後にプロスタサイクリンと呼ばれるPG-Xは、当時知られていた他の抗凝集剤の30倍の効力を持っていた。
1976年、ベインはサルバドール・モンカダ、リシャード・グリグルフスキー、スチュアート・バンティングらと共同で、プロスタサイクリンに関する最初の論文を『Nature』誌に発表した。この共同研究により、合成された分子が生まれ、エポプロステノールと名付けられた。しかし、天然のプロスタサイクリンと同様に、エポプロステノールの分子は溶液中では不安定で、すぐに分解されてしまう。
関連項目
外部リンク
- “Epoprostenol”. Drug Information Portal. U.S. National Library of Medicine. 2021年8月26日閲覧。
- “Epoprostenol sodium”. Drug Information Portal. U.S. National Library of Medicine. 2021年8月26日閲覧。