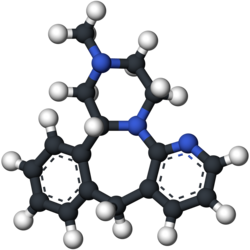
ミルタザピン

| |
| |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 胎児危険度分類 |
|
| 法的規制 | |
| 投与方法 | 経口 |
| 薬物動態データ | |
| 生物学的利用能 | 49.7% |
| 代謝 | 肝臓 (CYP1A2,CYP2D6,CYP3A4) |
| 半減期 | 23~33時間 |
| 排泄 | 代謝物として:尿中75%、糞中15% |
| 識別 | |
|
CAS番号 |
61337-67-5 |
| ATCコード | N06AX11 (WHO) |
| PubChem | CID: 4205 |
| DrugBank | DB00370 |
| ChemSpider | 4060 |
| KEGG | D00563 |
| 化学的データ | |
| 化学式 | C17H19N3 |
| 分子量 | 265.35 g/mol |
| |
| 物理的データ | |
| 融点 | 114 - 116 °C (237 - 241 °F) |
| 水への溶解量 | メタノール、エタノールに溶ける mg/mL (20 °C) |
ミルタザピン(Mirtazapine)は、オランダのオルガノン社(前シェリング・プラウ社、現メルク社)が創製した四環系抗うつ薬。ノルアドレナリン作動性・特異的セロトニン作動性抗うつ薬 (NaSSA) というカテゴリに分類される。SSRIやSNRIとは異なる作用機序であり、短時間で効果が発現し、効果は持続的である。
2009年3月現在、93カ国で承認され、日本においては、2009年7月に、医薬品医療機器総合機構から製造販売が承認され、MSD(旧シェリング・プラウ)からレメロン、Meiji Seika ファルマからリフレックスという商品名で販売されている。
適応症
- うつ病およびうつ状態
作用機序
- NaSSAのSSRIやSNRIとの決定的な違いは、神経伝達物質受容体に対する親和性の高さである。
- 既存のSSRIやSNRIは各神経伝達物質受容体に対しての親和性が低く、モノアミン再取り込みポンプの阻害によりその薬理作用を発現させていた。
- ミルタザピンは、シナプス前膜にあるα2受容体(自己受容体とヘテロ受容体)に対してアンタゴニストとして作用し、ノルアドレナリンとセロトニン(5-HT)の神経伝達を増強する。また、5-HT2受容体と5-HT3受容体を遮断する作用があるため、抗うつ作用に関連する5-HT1A受容体のみを特異的に活性化することによって抗うつ効果を発揮する。このため、ノルアドレナリン作動性・特異的セロトニン作動性抗うつ薬(NaSSA:Noradrenergic and Specific Serotonergic Antidepressant)と呼ばれる。ミルタザピンは、日本で初めてプラセボ対照比較試験においてプラセボに対する優越性を検証した抗うつ薬である。
- 作用機序が違うため難治性うつ病に対しSNRI、もしくはSSRIと併用するカリフォルニア・ロケットという投薬がされる場合がある。
副作用
5-HT2受容体と5-HT3受容体の遮断作用を持つため、SSRIと比較して嘔気・嘔吐、性機能障害などの副作用が少ない。一方、H1受容体遮断作用が強いため鎮静系の副作用が目立つ。
主な副作用
- 日本での臨床試験における主な副作用は以下のとおり。
- 傾眠:50.0%、口渇:20.6%、倦怠感:15.2%、便秘12.7%、アラニン・アミノトランスフェラーゼ(ALT)増加12.4%
終了時
ミルタザピンとその他の抗うつ薬は終了時に離脱症状を起こす。離脱症状は多くの向精神薬に共通していることに注意すべきであるが、それはいくつかのベンゾジアゼピンよりは重篤ではない。離脱症状を最小化するために、徐々にゆっくりとした減薬が推奨される。ミルタザピン治療の突然の中断の影響は、抑うつ・不安・パニック発作・めまい・落ち着きのなさ・短気・食欲減退・不眠・下痢・吐き気・嘔吐・アレルギーや瘙痒などのインフルエンザ様症状・頭痛・時に軽躁病/躁病がある。
性差
日本での臨床試験において、男女いずれかで5%以上かつ男女差が2倍以上発現した副作用事象を抽出したところ、要因は明確になっていないが、体重増加・食欲亢進、便秘について女性における発現率が高く、それ以外の事象については明らかな差異は認められなかった。
ミルタザピン長期投与群(n = 男性58 vs 女性51)で、体重増加の副作用発現は男性4(6.9%) vs 女性11(21.6%)、食欲亢進の副作用発現は男性0(0%) vs 女性4(7.8%)。
重大な副作用
重大な副作用は以下のとおり(頻度不明)。
禁忌
- ミルタザピンに対して過敏症の既往歴のある患者
- MAO阻害剤を投与中あるいは投与中止後2週間以内の患者
薬物相互作用
ミルタザピンのシトクロムP450の阻害能は最小限であり、薬物相互作用は比較的少ないとされる。
併用禁忌
併用注意
- CYP3A4阻害剤(HIVプロテアーゼ阻害剤、アゾール系抗真菌薬、エリスロマイシンなど):ミルタザピンの血漿中濃度が増大する可能性がある。
- CYP3A4誘導剤(カルバマゼピン、フェニトイン、リファンピシンなど):ミルタザピンの血漿中濃度が減少する可能性がある。
- シメチジン:CYP1A2、CYP2D6、CYP3A4 などへの阻害作用により、ミルタザピンの血漿中濃度が増大する可能性がある。
- 鎮静剤(ベンゾジアゼピン系薬剤など):相加的な鎮静作用が考えられる。
- 飲酒:相加的・相乗的な鎮静作用が考えられる。
毒性
単回投与毒性
| 動物種 | 投与経路 | 概略の致死量(mg/kg) |
|---|---|---|
| マウス | 経口 | 雄500,雌550 |
| ラット | 経口 | 雄400,雌281 |
反復投与毒性
| 動物種 | 投与期間 | 投与経路 | 投与量(mg/kg/日) | 無毒性量(mg/kg/日) |
|---|---|---|---|---|
| ラット | 13週 | 経口 | 10,40,120 | 40 |
| ラット | 52週 | 経口 | 2.5,20,120 | 20 |
| イヌ | 13週 | 経口 | 5,20,80 | 80 |
| イヌ | 52週 | 経口 | 2.5,15,80 | 80 |
販売名
ミルタザピンは、日本においてリフレックス(Reflex、Meiji Seika ファルマ)、レメロン(Remeron、シェリング・プラウ)の商標で販売されている。国外では、レメロン、ミルタザピンなどの商品名が多い。
後発医薬品はミルタザピン錠「製薬会社名」の名称で複数の製薬会社が製造・販売している。
参考文献
- “シェリング・プラウ 『医薬品インタビューフォーム:レメロン錠15mg』” (PDF). シェリング・プラウ公式サイト (2009年9月作成改訂第2版). 2009年1月10日閲覧。。
| ||||||||||||
| ||||||||||||