キメラ抗原受容体
キメラ抗原受容体(キメラこうげんじゅようたい、英: Chimeric antigen receptor; 略称: CAR、キメラ免疫受容体、キメラT細胞受容体、人工的T細胞受容体)は、遺伝子編集(ゲノム編集)を行うことで工学的につくられた人工の受容体である。
概要
キメラ抗原受容体T細胞(CAR-T細胞)は、キメラ抗原受容体を生産するように遺伝子操作されたT細胞である。任意の抗原に特異的なキメラ抗原受容体遺伝子が、リンパ球免疫のエフェクター細胞(T細胞)に導入される。 通常、これらの受容体は、モノクローナル抗体の特異性を持ち、T細胞へはレトロウイルス・ベクターなどより遺伝子が導入される。この受容体は異なる起源からなるいくつかの遺伝子から構成されているため「キメラ」と呼ばれる。
ペンシルベニア大学のカール・ジューンらによって開発されたCAR-T療法はCAR-T細胞をがん治療に用いる。CAR-T療法はアメリカ食品医薬品局 (FDA) により急性リンパ性白血病に対して承認された。T細胞は患者から取り出され、遺伝子改変され、患者の特定のがんに対して特異的な受容体を過剰発現するようになる。このT細胞は癌を認識し、癌細胞を殺せるようになり、患者の体内に戻される(養子細胞移植)。ドナー以外の患者への投与については研究段階にある。
FDAは、2017年8月にtisagenlecleucel(製品名Kymriah、ノバルティス製造販売)を急性リンパ芽球性白血病の治療に承認した。日本の第一三共も「びまん性大細胞性B細胞性リンパ腫 (DLBCL)」に対して開発を行っている。
構造
最も一般的なCARは、モノクローナル抗体由来の単鎖可変領域フラグメント (scFv)と CD3-ζ膜貫通部ドメインおよび細胞内ドメインを融合させたものである。 たとえば、14g2a-ζは、ハイブリドーマ14g2a(これはジシアロガングリオシドGD2を認識する)から由来したscFvとの融合タンパク質である。
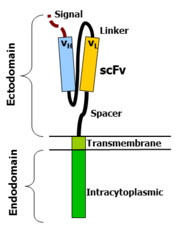
免疫グロブリンの変異部は重鎖および軽鎖からなり、2つの抗原認識部位を持つ。キメラ抗原受容体では、柔軟なリンカーにより重鎖可変領域VHと軽鎖可変領域VLを結合し単鎖可変領域フラグメント(scFv)を形成する。柔軟なスペーサーは、scFvに異なる方向での抗原結合を許容する。 膜貫通ドメインは、典型的な疎水性のαヘリックスタンパク質であり、本来の分子が細胞内ドメインに送るものと同様の信号を送る。
I型タンパク質は、二つのタンパク質ドメインが膜貫通αヘリックスタンパクによりつながれている。 細胞膜の脂質二重層を膜貫通ドメインが貫通し、細胞膜が細胞内と細胞外を分けている。 細胞外ドメインにあるタンパク質が結合し、細胞内ドメインが変化することは、この受容体が抗原を認識し、細胞内へ信号を送ることとなる。
ScFv/CD3-ζハイブリッドは、scFvが抗原を認識し、ζ信号を伝達する。 T細胞がこの分子を発現させたとき(一般的に癌レトロウイルスベクターによる形質導入)、形質導入T細胞は標的細胞の発現するGD2(例: 神経芽腫細胞)を認識し殺傷する。 悪性B細胞を対象として、B細胞の表面マーカーであるCD19特異的なキメラ抗原受容体が研究されている。
細胞外ドメイン
細胞外ドメインは、膜タンパク質のうち細胞の外にある部分を指す。細胞質の外であり、細胞外空間に曝露されている。細胞表面の受容体 やタンパク質は、細胞外空間から信号を受け取るため、細胞外空間に細胞外ドメインを曝さなくてはならない。
信号ペプチド
信号ペプチド は粗面小胞体が作る新生タンパク質である。受容体はグリコシル化され、細胞膜に定着するかどうかが重要である。 真核生物の信号ペプチドは種を超えて作用する。 一般的に、信号ペプチドはアミノ末端(N末端)側の部分に結合する。例えば、scFvでの軽鎖-リンカー-重鎖であれば、軽鎖の信号が用いられる。
抗原認識領域
抗原認識 領域は一般的にscFvが用いられるが、多くの派生種がある。 抗原認識ドメインは、 T細胞受容体 (TCR) のαとβシングルチェーンから得られる。単純な細胞外ドメインにとして(例: CD4の細胞外ドメインはHIVに感染した細胞を認識する)や、サイトカイン 認識部分(サイトカイン受容体から得られる)などがある。 高い親和性を持つものが、抗原認識部位として用いられる。
スペーサー
スペーサー領域は、抗原結合ドメインと膜貫通ドメインを繋いでいる。 十分に柔軟であるため、抗原結合ドメインが抗原認識するため、さまざまな方向に向くことができる。 最も単純な形態は、IgG1から得られたヒンジ領域である。 代わりに免疫グロブリンのCH2CH3領域とCD3の一部を含むものもある。 ほとんどがscFv構造を用いるが、IgG1のヒンジでも十分である。 しかし、最良のスペーサーは多くの場合経験的に決定される。
膜貫通ドメイン
膜貫通ドメインは疎水性のαヘリックスからなる。 一般的には、膜貫通ドメインには、細胞内ドメインの細胞膜に最も近い部分を用いる。 興味深いことに、人工TCRは本来のTCRに比べ、CD3-ζ膜貫通ドメインがアスパラギン酸残基での荷電に依存する。 異なる膜貫通ドメインは、異なる受容体安定性を持つ。 CD28膜貫通ドメインは明瞭に発現し、安定した受容体である。
細胞内ドメイン
この受容体の最終的な機能部分である。 抗原認識した後、受容体は集合し、信号は細胞内へ伝達される。 最も一般的に使用される細胞内ドメインはCD3-ζであり、3つのITAMを持つ。 T細胞が抗原に結合した後に、活性化信号は伝達される。 CD3-ζが提供養を活性化信号との共刺激シグナル伝達が必要です。 例えば、キメラ抗CD28とOX40で使用できCD3-ζを送信する増殖/生存の信号を採用しているため、新しい種類のを使用することができます。
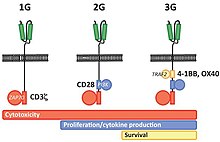
CAR-Tデザインの進化
第一世代のCARでは、細胞内ドメインにはT細胞受容体の細胞内シグナルを伝達するCD3ζ-チェーンから得たものを用いていた。 第二世代CARでは、種々の共刺激タンパク質受容体から得た細胞内信号ドメインが細胞内の部位に追加されている(例: CD28、41BB、ICOS)。前臨床研究では、第二世代のCARは、T細胞の抗腫瘍活性を改善させた。 第三代のCARではさらに効果を増すため、複数の信号伝達ドメインを繋いでいる(CD3ζ-CD28-41BBやCD3ζ-CD28-OX40など)。
CAR治療の進化は、基礎研究から臨床応用への良い例である。 PI3K結合部位はCD28の共受容体であると同定された。ITAMモチーフは、CD4-lckまたは D8-p56lck複合体の対象であることが同定された。
Strep-tag II配列(Trp-Ser-His-Pro-Gln-Phe-Glu-Lysというポリペプチド配列。これは ストレプトアビジンに親和性がある)を合成したCARの特定の部位に挿入し、これを持つT細胞だけを取り出す。スペーサー長を最適にし、抗体でコーティングされ、マイクロビーズで集められ、大規模に必要なCAR-T細胞だけを集めることができる。 Strepタグを用いて、人工細胞を刺激し、急速に増殖させることができる。 Strepタグに結合する抗体を用いることで、人工細胞を200倍まで増やすことができる。既存の方法とは異なり、この技術によりがん特異的T細胞のみを増やすことができる。
Prime CAR-T細胞
Prime CAR-T細胞では、IL-7と呼ばれるサイトカインとCCL19と呼ばれるケモカインの両方を同時に産生する。この結果、固形癌に対しても宿主の免疫応答を活性化することで、従来のCAR-T療法よりも強力な治療が可能になると期待されている。
SMDCアダプタ技術
SMDCs(small molecule drug conjugates; 小分子の薬物結合体)プラットフォームは腫瘍免疫領域では新しくまた実験的なアプローチを可能にする、この技術はFITCなどの小分子に対する親和性を極端に高くすることができる。 これらの細胞が様々な種類のがんに用いられ、二重特異性SMDCアダプター分子と同時に作用する。 これらの二重特異性アダプターを構築しFITC分子腫瘍ホーミング分子を精密に橋のユニバーサル車T細胞のがん細胞の原因となる局所のT細胞活性化します。 抗腫瘍活性をマウスで誘導しながら、限られた時間での準備のユニバーサル車T細胞の正しい抗原特異的アダプター分子が存在します。 抗腫瘍活性や毒性を制御できる調整により投与しアダプター分子を注入します。 処理のantigenicallyの不均質性腫瘍に達成できる投与による混合物、希望する抗原特異的アダプタです。 以下のような課題がCAR-T細胞療法には残されている:
- サイトカイン放出や腫瘍崩壊の程度を制御できない
- 癌を駆除してしまった後に、「スイッチを切る」ことができない
- 腫瘍に特異的な抗原に対して、対応するCAR-T細胞がひとつひとつ作る必要がある
これらは新しい技術でいずれ解決される可能性がある。
臨床研究
CARの臨床応用としては、T細胞抗原受容体をベクター (例えばウイルス)を用いて悪性腫瘍に特異的なものに変えることがある。 前臨床および 臨床試験に て構造と信号伝達を最適なものとすることが焦点となっている。
安全上の懸念
CAR-T細胞治療は、独特な有望ながん治療であるが、重大な安全上の懸念が残されている。 臨床試験では、CARによる潜在的な毒性が明らかになった。健康な組織で腫瘍細胞と同じ抗原を持っているものは攻撃対象となり、移植片対宿主病 (GVHD)と同様な結果を生む。 この問題は、自殺遺伝子 をCAR-T細胞に導入することで解決する可能性がある。 プロドラッグ投与により自殺遺伝子が活動するよう設計し、GVHDを起こすと、CAR-T細胞がアポトーシスにより死滅するようにできる。