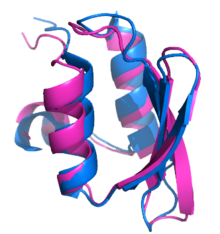Rosetta@home

| |

| |
| 作者 | Baker laboratory, University of Washington; Rosetta Commons |
|---|---|
| 初版 | 2005年10月6日 (2005-10-06) |
| 最新版 |
Rosetta: 4.20
/ 2020年5月1日 (2020-05-01)
Rosetta Mini: 3.78 / 2017年10月3日 (2017-10-03) Rosetta for Android: 4.20 / 2020年5月1日 (2020-05-01) |
| 対応OS | Windows, macOS, Linux, Android |
| プラットフォーム | BOINC |
| 対応言語 | 英語 |
| サポート状況 | Active |
| 種別 | 分散コンピューティング |
| 公式サイト |
boinc |
Rosetta@home(ロゼッタ・アット・ホーム、R@h)は、ワシントン大学のデイヴィッド・ベイカー教授の研究室が運営するBOINCプラットフォーム上のタンパク質構造予測を研究するためのボランティア・コンピューティングプロジェクトである。
概要
Rosetta@homeは、2022年3月14日時点で平均73,712.4 G(ギガ)FLOPS(フロップス)以上の処理能力を持つ約6万3,000台のアクティブなボランティアコンピュータの助けを借りて、タンパク質-タンパク質ドッキング (英語版) を予測し、新しいタンパク質を設計することを目的としている。 Rosetta@Home のビデオゲームである Foldit は、クラウドソーシングのアプローチでこれらの目標を達成することを目指している。 プロジェクトの多くは、プロテオミクス手法の精度とロバスト性を向上させるための基礎研究に重点を置いているが、Rosetta@homeはマラリアやアルツハイマー病などの応用研究も行っている。
他の BOINC プロジェクトと同様に、Rosetta@home は、ボランティアのコンピュータからの未使用時の計算処理資源を使用して、個々の作業単位(ワークユニット) (英語版) の計算を実行する。完成した結果は中央のプロジェクトサーバーに送られ、そこで検証され、プロジェクトデータベースに統合される。このプロジェクトはクロスプラットフォームで、さまざまなハードウェア構成で動作する。ユーザは、個々のタンパク質構造予測の進捗状況を Rosetta@home スクリーンセーバーで確認することができる。
タンパク質の構造予測の問題は、Googleが所有するDeepMindが人工知能を使用して既に解決している。DeepMindは、タンパク質の構造を最も正確に予測するために、Rosettaの入力を他の多くのデータに取り入れた予測ツールAlphaFoldを開発した。AlphaFoldは、タンパク質構造予測技術精密評価(CASP)コンテストでRosettaを追い抜き、タンパク質の配列データを持つ約100万の生物種から2億以上のタンパク質の構造を予測するのに成功し、実質的にタンパク質宇宙を網羅した。すべての予測結果を含む構造データベースは、DeepMindと欧州バイオインフォマティクス研究所によって共同で構築された。
疾患関連の研究に加えて、Rosetta@homeネットワークは、構造バイオインフォマティクスの新しい手法のテストフレームワークとしても機能する。そのような手法は、RosettaDock やヒトプロテオーム・フォールディング・プロジェクト (英語版) 、マイクロバイオーム免疫プロジェクトなどの Rosetta ベースの他のアプリケーションで使用され、Rosetta@home の大規模で多様なボランティアコンピュータで十分に開発され、安定していることが証明された後に使用される。Rosetta@home で開発された新しい手法の特に重要なテストは、タンパク質構造予測技術精密評価(CASP)とタンパク質間相互作用予測精密評価(CAPRI)実験であり、2年に1度の実験で、それぞれタンパク質構造予測とタンパク質-タンパク質ドッキング予測の最先端の状態を評価する。Rosetta@homeは常に主要なドッキング予測器の中にランク付けされており、利用可能な最高の三次構造予測器の一つである。
新型コロナウイルス感染症(COVID-19)の原因ウイルスSARS-CoV-2の解析プロジェクトに参加したいという新規ユーザの流入に伴い、Rosetta@homeは2020年3月28日時点で最大1.7ペタフロップスまで計算能力を向上させた。2020年9月9日、Rosetta@homeの研究者は、SARS-CoV-2に対する10種の強力な抗ウイルス剤候補を説明する論文を発表した。Rosetta@homeはこの研究に貢献し、これらの抗ウイルス剤候補は、第1相臨床試験 (2022年初頭に開始される可能性がある) に向かっている。Rosetta@homeチームによると、Rosettaのボランティアはナノ粒子ワクチンの開発に貢献した。このワクチンはライセンスされ、2021年6月に第I/II相臨床試験を開始したIcosavaxのIVX-411と、SK Bioscienceが開発中で、韓国ですでに第III相臨床試験が承認されている(Skycovione) GBP510として知られている。
また、Institute of Protein Design (IPD) で初めて作成され、2019年1月に論文発表された抗がん剤候補のNL-201は、IPDからスピンオフしたNeoleukin Therapeuticsの支援を受けて、2021年5月に第1相ヒト臨床試験を開始した。Rosetta@homeはNL-201の開発で役割を果たし、タンパク質設計の検証に役立つ「フォワードフォールディング」実験で貢献した。
コンピューティング・プラットフォーム
Rosetta@home アプリケーションと BOINC 分散コンピューティングプラットフォームは、Windows、Linux、macOS の各 OS で利用可能である。 BOINC は、FreeBSD のような他のオペレーティングシステムでも動作する。Rosetta@homeに参加するには、クロック速度500MHz以上の中央処理装置(CPU)、200メガバイトの空きディスク容量、512メガバイトの物理メモリ、インターネット接続が必要である。2017年10月3日現在、Rosetta Miniアプリケーションの現在のバージョンは3.78である。現在の推奨BOINCプログラムバージョンは7.6.22である。ユーザーの BOINC クライアントとワシントン大学の Rosetta@home サーバー間の通信には標準ハイパーテキスト転送プロトコル (HTTP) (ポート80) が使用され、パスワード交換時には HTTPS (ポート443)が使用される。BOINC クライアントのリモートおよびローカル制御ではポート 31416 とポート 1043 を使用しているが、これらはファイアウォールの内側にある場合は特にブロック解除を要する可能性がある。個々のタンパク質のデータを含むワークユニット (英語版) は、ワシントン大学のBaker研究室にあるサーバーからボランティアのコンピュータに配信され、割り当てられたタンパク質の構造予測を計算する。与えられたタンパク質の構造予測の重複を避けるために、各ワークユニットはランダムなシード番号 (英語版) で初期化される。これにより、各予測は、タンパク質のエネルギー地形に沿って下降するユニークな軌跡を得ることができる。Rosetta@home からのタンパク質構造予測は、与えられたタンパク質のエネルギーランドスケープにおけるグローバルな最小値の近似値である。このグローバルな最小値は、タンパク質の最もエネルギー的に有利なコンフォメーション、すなわちネイティブな状態 (英語版) を表す。
Rosetta@home グラフィカル・ユーザー・インターフェース(GUI)の主な機能は、シミュレーションされたタンパク質の折り畳みプロセス中の現在のワークユニットの進行状況を表示するスクリーンセーバーである。スクリーンセーバーには次が表示される:
- タンパク質の構造
- (左上) ターゲットとなるタンパク質が、最も低いエネルギーの構造を求めて様々な形状(コンフォーメーション)に変化している様子
- (中央上) 最近の構造
- (右上) 現在の最も低いエネルギーの構造
- (その下) すでに決定されている場合は真の構造
- グラフ
他のBOINCプロジェクトと同様に、Rosetta@homeは、ホストOSのアカウントにログインする前に、アイドル状態のコンピュータの電力を使って、ユーザのコンピュータのバックグラウンドで実行される。プログラムは、他のアプリケーションが必要とする CPU からリソースを解放し、通常のコンピュータの使用に影響を与えない。多くのプログラム設定は、ユーザーアカウントの環境設定を介して指定することができる。プログラムが使用できる CPU リソースの最大割合(持続的な容量で実行されているコンピュータの消費電力や発熱を制御するため)、プログラムを実行できる 1 日の時間帯、その他多くの設定がある。
Rosetta@home ネットワーク上で動作するソフトウェアである Rosetta は、Fortran で書かれたオリジナルバージョンよりも開発が容易になるように C++ で書き直された。この新バージョンはオブジェクト指向で、2008年2月8日にリリースされた。ロゼッタコードの開発はロゼッタコモンズによって行われている。このソフトウェアはアカデミックコミュニティに自由にライセンスされており、製薬会社には有償で提供されている。
プロジェクトの意義
ゲノム配列決定プロジェクト (英語版) の普及により、科学者は細胞内で機能を果たす多くのタンパク質のアミノ酸配列(一次構造)を推測することができるようになった。タンパク質の機能をよりよく理解し、合理的なドラッグデザインを支援するためには、科学者はタンパク質の3次元3次構造を知る必要がある。
タンパク質の立体構造は、現在、X線結晶構造解析または核磁気共鳴(NMR)分光法を用いて実験的に決定されている。このプロセスは時間がかかり(タンパク質を初めて結晶化する方法を見つけるのに数週間から数ヶ月かかることもある)、コストがかかる(タンパク質1個あたり約10万ドル)。 残念ながら、新しい配列が発見される速度は構造決定の速度をはるかに上回っている。アメリカ国立生物工学情報センター(NCBI)の非冗長(NR)タンパク質データベースで利用可能な7,400,000以上のタンパク質配列のうち、タンパク質の3次元構造が解決され、タンパク質の構造情報の主要なリポジトリである蛋白質構造データバンク (英語版) に寄託されているのは52,000未満である。Rosetta@homeの主な目標の一つは、既存の手法と同等の精度で、時間とコストを大幅に削減した方法でタンパク質の構造を予測することである。 また、Rosetta@homeは、X線結晶構造解析やNMR分光法などの従来の手法では解析が非常に困難であるにもかかわらず、現代の医薬品のターゲットの大部分を占めている膜タンパク質(Gタンパク質共役型受容体(GPCR)など)の構造とドッキングを決定する方法も開発している。
タンパク質構造予測の進歩は、年2回、世界中の研究者がタンパク質のアミノ酸配列からタンパク質の構造を導き出そうとする「タンパク質構造予測技術精密評価」(CASP)で評価される。 この実験で高得点を獲得したグループは、競争の激しい実験であり、タンパク質の構造予測の技術的水準を示す事実上の旗手とされている。 Rosetta@homeのベースとなっているRosettaは、2002年のCASP5から使用されている。 2004年のCASP6実験では、CASPターゲットT0281の提出モデルにおいて、原子レベルに近い分解能で第一原理(ab initio)計算によるタンパク質構造予測を初めて実現し、歴史に名を刻んだ。第一原理モデリングは、構造相同性からの情報を利用せず、配列相同性からの情報に依存し、タンパク質内の物理的相互作用をモデル化しなければならないため、タンパク質の構造予測の中でも特に難しいカテゴリーと考えられている。 Rosetta@homeは2006年からCASPで使用されており、CASP7では構造予測のすべてのカテゴリーでトップの予測器の一つとなっている。これらの高品質な予測は、Rosetta@homeのボランティアが提供してくれた計算能力によって可能になった。計算能力の向上により、Rosetta@home はより多くの領域の構造空間 (英語版) (タンパク質が想定しうる形状)をサンプルすることが可能になり、Levinthal のパラドックス (英語版) によれば、タンパク質の長さが長くなると指数関数的に増加すると予測されている。
Rosetta@homeは、複数の複合タンパク質または四次構造 (英語版) の構造を決定するタンパク質-タンパク質ドッキング (英語版) 予測にも使用されている。 この種のタンパク質相互作用は、抗原抗体や酵素阻害剤の結合、細胞内外間の輸送など、多くの細胞機能に影響を与える。 これらの相互作用を決定することは、医薬品設計にとって非常に重要である。
Rosettaは「タンパク質間相互作用予測精密評価」(CAPRI) 実験に使用されており、CASPがタンパク質構造予測の進歩を評価するのと同様に、タンパク質ドッキング分野の状態を評価する。 Rosetta@home のプロジェクトボランティアによって提供された計算能力は、CAPRI での Rosetta のパフォーマンスの主な要因として挙げられており、そのドッキング予測は最も正確で完全なものの一つとなっている。
2008年初頭、Rosettaは自然界では観測されたことのない機能を持つタンパク質を計算で設計するために使用された。これは、2004年に発表された、天然型に比べて酵素活性が向上したタンパク質を計算で設計したという注目を集めていた論文が撤回されたことに端を発している。このタンパク質がどのようにして作られたかを説明した David Baker 氏のグループの 2008 年の研究論文は、Rosetta@home が利用可能な計算機リソースを引用したもので、このタンパク質設計法の重要な概念の証明となった。この種のタンパク質設計は、将来的には創薬、グリーンケミストリー、バイオレメディエーションなどへの応用が期待されている。
疾患関連研究
タンパク質の構造予測、ドッキング、デザインなどの基礎研究に加えて、Rosetta@homeは疾病関連の研究にも利用されている。David Baker氏のRosetta@homeジャーナルには、多数のマイナー研究プロジェクトが掲載されている。2014年2月現在、フォーラムでは、最近の出版物の情報や簡単な説明が更新されている。2016年以降、フォーラムのスレッドは使用されなくなり、研究に関するニュースはプロジェクトの一般的なニュースセクションで見つけることができる。
アルツハイマー病
Rosetta ソフトウェアスイートのコンポーネントである RosettaDesign を使用して、アミロイド原性タンパク質のどの領域がアミロイド様フィブリル (英語版) を形成する可能性が高いかを正確に予測した。興味のあるタンパク質のヘキサペプチド(6アミノ酸長のフラグメント)を取り出し、既知のフィブリルを形成するヘキサペプチドと類似した構造に最も低いエネルギーで一致するものを選択することで、RosettaDesignは、ランダムなタンパク質の2倍の確率でフィブリルを形成するペプチドを特定することができた。Rosetta@homeは、アルツハイマー病の原因とされるフィブリル形成タンパク質であるアミロイドβの構造予測にも使用された。ロゼッタが設計したタンパク質については、フィブリルの形成を防ぐ可能性のある予備的な結果が得られているが、アルツハイマー病を予防できるかどうかは不明である。
炭疽菌
Rosettaのもう一つのコンポーネントであるRosettaDockは、炭疽菌毒素 (英語版) を構成する3つのタンパク質 (致死因子(LF)、浮腫因子(EF)、保護抗原(PA))間の相互作用をモデル化するために、実験的手法と組み合わせて使用された。 このコンピュータモデルは、LFとPAのドッキングを正確に予測し、それぞれのタンパク質のどのドメインがLFとPAの複合体に関与しているかを明らかにした。この洞察は最終的に炭疽菌ワクチンの改良につながる研究に利用された。
単純ヘルペスウイルス1型
RosettaDockは、抗体 (免疫グロブリンG)と、抗ウイルス抗体を分解する役割を果たす単純ヘルペスウイルス1型 (HSV-1) が発現する表面タンパク質との間のドッキングのモデル化に使用された。 RosettaDockによって予測されたタンパク質複合体は、特に入手が困難な実験モデルと密接に一致しており、研究者らは、このドッキング法が、X線結晶学がタンパク質-タンパク質界面のモデル化で抱えている問題のいくつかを解決する可能性があると結論づけた。
HIV
ビル&メリンダ・ゲイツ財団による19.4百万ドルの助成金を受けた研究の一環として、Rosetta@homeは、ヒト免疫不全ウイルス(HIV)のための複数の可能性のあるワクチンの設計に使用されている。
マラリア
「グローバルヘルスにおけるグランドチャレンジ」 (英語版) イニシアティブの研究では、Rosetta を使用して、ガンビエ・ハマダラ蚊 (Anopheles gambiae) を根絶したり、蚊がマラリアを感染させないようにすることができる、新しいホーミングエンドヌクレアーゼタンパク質を計算機的に設計している。ホーミングエンドヌクレアーゼのように、タンパク質とDNAの相互作用を具体的にモデル化して変化させることができるため、Rosettaのような計算科学的タンパク質設計法は、遺伝子治療(がん治療の可能性を含む)において重要な役割を果たすことになる。
COVID-19
Rosetta分子モデリングスイートは最近、SARS-CoV-2スパイクタンパク質の原子スケールの構造を、実験室で測定する数週間前に正確に予測するために使用された。2020年6月26日、同プロジェクトは、実験室でSARS-CoV-2ウイルスを中和する抗ウイルスタンパク質の作成に成功し、これらの実験的な抗ウイルス薬が動物実験の試験に向けて最適化されていることを発表した。
その後、10種類のSARS-CoV-2ミニタンパク質阻害剤を説明する論文が9月9日、Science誌に掲載された。これらの阻害剤のうち2つ、LCB1とLCB3は、SARS-CoV-2に対して開発されている最高のモノクローナル抗体よりも、モル比、質量ともに数倍以上の効力があるという。さらにこの研究では、これらの阻害剤は高温下でも活性を保持し、抗体よりも20倍小さく、したがって潜在的な中和活性部位を20倍多く有し、局所投与での薬効を高めることを示唆している。本阻害剤のサイズが小さく、安定性が高いことから、経鼻的に塗布するゲル製剤や、または呼吸器系に直接投与する粉末として適切なものになると期待されている。研究チームは、今後、これらの阻害剤を治療薬や予防薬として開発することを目指している。2021年7月現在、これらの抗ウイルス剤候補は2022年初頭に臨床試験を開始すると予測されており、前臨床試験および初期臨床試験のためにビル&メリンダ・ゲイツ財団から資金提供を受けていた。動物実験では、これらの抗ウイルス剤候補は、アルファ、ベータ、ガンマなどの懸念される変異種に有効であった。
Rosetta@homeは、計算によって設計された200万個以上のSARS-CoV-2 スパイク結合タンパク質のスクリーニングに使用され、この研究に貢献した。
がん
Rosetta@homeの研究者は、受容体のαサブユニットと相互作用しない、Neoleukin-2/15 (ネオロイキン-2/15) と呼ばれるIL-2受容体アゴニストを設計した。このような免疫シグナル分子は、がん治療に有用である。天然のIL-2はαサブユニットとの相互作用による毒性に悩まされるが、少なくとも動物モデルでは、設計されたタンパク質の方がはるかに安全である。Rosetta@homeは、設計の検証に役立った「フォワードフォールディング実験」に貢献した。
2020年9月のNew Yorker紙の特集で、David Baker氏は、Neoleukin-2/15のヒトによる臨床試験を「今年後半」に開始すると述べている。Neoleukin-2/15は、Baker研究室からのスピンオフ企業であるNeoleukinによって開発されている。2020年12月、Neoleukinは、Neoleukin-2/15 (指定: NL-201) の第1相臨床試験の開始に向けて、アメリカ食品医薬品局(FDA)に治験薬申請を行うと発表した。オーストラリアでも同様の申請を行っており、ネオロイキンは第1相臨床試験に120名の参加者を登録したいとしている。
開発の歴史と分科
Rosettaは、1998年にBaker研究室によって第一原理計算による構造予測のためのアプローチとして導入されのが始まりで、それ以来、いくつかの開発ストリームと独自のサービスへと発展してきた。 Rosettaプラットフォームの名前は、タンパク質のアミノ酸配列の構造的な「意味」を解読しようとする「ロゼッタ・ストーン」に由来している。Rosettaの登場から7年以上が経過し、2005年10月6日にRosetta@homeプロジェクトがリリースされた(つまり、ベータ版ではなくなったと発表された)。Rosettaの初期開発に携わった大学院生やその他の研究者の多くは、その後、他の大学や研究機関に移っており、その後、Rosettaプロジェクトのさまざまな部分を強化してきた。
RosettaDesign

RosettaDesign(ロゼッタデザイン)は、Rosettaをベースにしたタンパク質設計のための計算機的アプローチで、2000年にはプロテインGの折り畳み経路の再設計の研究から始まった。 2002年にはRosettaDesignを用いて、これまで自然界で記録されたことのない全体的な折り畳み (英語版) を持つ93アミノ酸長のα/βタンパク質 Top7を設計した。 この新しい構造は、Rosettaによって、X線結晶構造解析によって決定された構造のRMSDが1.2Å以内であることが予測され、これは非常に正確な構造予測であることを示している。RosettaとRosettaDesignは、このような長さの新しいタンパク質の構造を設計し、正確に予測した最初の研究者として広く知られるようになったが、この二重のアプローチを説明した2002年の論文は、ジャーナル「Science」に2つのポジティブレターを掲載し、他の240以上の科学論文で引用された。この研究の成果物であるTop7は、2006年10月にRCSB PDBの「Molecule of the Month」として取り上げられ、その予測結晶構造とX線結晶構造のそれぞれのコア(残基60〜79)を重ね合わせたものが、Rosetta@homeのロゴとして掲載されている。
Brian Kuhlman氏は、元David Baker研究室で博士号を取得し、現在はノースカロライナ大学チャペルヒル校の准教授として、RosettaDesignをオンラインサービスとして提供している。
RosettaDock
RosettaDock (ロゼッタドック)は、2002 年の最初の CAPRI 実験の際に、Baker 研究室の蛋白質-蛋白質ドッキング予測のためのアルゴリズムとして Rosettaソフトウェアに追加された。この実験では、RosettaDock は、連鎖球菌の化膿性エキソトキシンA と T細胞受容体β鎖とのドッキングを高精度で予測し、ブタの α-アミラーゼとラクダ科(Camelid, カメロイド)抗体との複合体を中精度で予測した。RosettaDock 法は、可能性のある7つの予測法のうち2つの精度の高い予測しかできなかったが、これは第1回CAPRI評価では19種類の予測法のうち7位にランク付けされるのに十分であった。
ワシントン大学在学中に RosettaDock の基礎を築いた Jeffrey Gray が、ジョンズ・ホプキンス大学に移ってからも、RosettaDock の開発は、その後のCAPRIラウンドに向けて2つの分岐点に分かれた。 Baker 研究室のメンバーは、Grayの不在の間にRosettaDockをさらに開発した。 2つのバージョンは、側鎖のモデル化、デコイ (英語版) の選択、その他の分野で若干の違いがあった。これらの違いにもかかわらず、BakerとGrayの両手法は、第2回CAPRI評価で30の予測グループの中でそれぞれ5位と7位にランクインし、良好な結果を残した。Jeffrey Gray氏のRosettaDockサーバーは、非商用利用のための無料ドッキング予測サービスとして提供されている。
2006年10月、RosettaDockはRosetta@homeに統合された。 この方法では、タンパク質のバックボーン (英語版) のみを使用した高速で粗いドッキングモデルのフェーズを使用した。 この段階では、相互作用する2つのタンパク質の相対的な配向、およびタンパク質-タンパク質界面での側鎖相互作用を同時に最適化して、最も低いエネルギーのコンフォメーションを見つけることができる。Rosetta@homeネットワークによる計算能力の大幅な向上と、バックボーンの柔軟性とループモデリング (英語版) のための修正されたフォールドツリー表現との組み合わせにより、RosettaDockは第3回CAPRI評価で63の予測グループのうち6位になった。
Robetta
Robetta (ロベッタ) (Rosetta Beta) サーバーは、Baker研究室が提供する非営利のab initioおよび比較モデリングのためのタンパク質構造予測の自動化サービスである。Robettaは、2002年のCASP5以来、年2回のCASP実験に自動予測サーバーとして参加しており、自動化サーバー予測カテゴリでは最高の成績を収めている。Robettaはそれ以降、CASP6とCASP7に参加し、自動化サーバと人間の予測グループの両方で平均以上の成績を収めている。 また、CAMEO3D (英語版) の連続評価にも参加している。
CASP6のタンパク質構造をモデル化する際、Robettaはまず、BLAST、PSI-BLAST、3D-Jury (英語版) を用いて構造的相同性を検索し、その配列をPfamデータベースの構造ファミリと照合することで、ターゲット配列を個々のドメイン、またはタンパク質の独立したフォールディングユニットに解析する。 次に、構造的相同性を持つドメインは、「テンプレートベースモデル」(すなわち、ホモロジーモデリング)プロトコルに従う。ここでは、Baker研究室内のアラインメントプログラム「K*sync」が相同配列のグループを生成し、これらのそれぞれがロゼッタde novo法によってモデル化され、デコイ(可能性のある構造)が生成される。 最終的な構造予測は、低分解能ロゼッタエネルギー関数によって決定された最も低いエネルギーのモデルを取ることによって選択される。 検出された構造的相同性を持たないドメインについては、生成されたデコイのセットから最も低いエネルギーモデルを最終的な予測値として選択するde novoプロトコルに従う。 これらのドメイン予測を連結して、タンパク質内のドメイン間、三次レベルの相互作用を調査する。 最後に、モンテカルロ構造探索プロトコルを用いて側鎖の寄与をモデル化する。
CASP8では、Rosettaの高分解能全原子精密化法を使用するようにRobettaが拡張されたが、これがないためにCASP7のRosetta@homeネットワークよりも精度が低いと言われていた。CASP11では、GREMLINと呼ばれる関連タンパク質の残基の共進化によるタンパク質コンタクトマップを予測する方法が追加され、より多くのde novoフォールドの成功を可能にした。
Foldit
2008年5月9日、Rosetta@homeのユーザーが分散コンピューティングプログラムの対話型バージョンを提案したことを受けて、Baker研究室は、Rosettaプラットフォームをベースにしたオンラインのタンパク質構造予測ゲームFolditを公開した。2008年9月25日の時点で、Folditの登録ユーザー数は59,000人を超えている。このゲームでは、ユーザーは、ターゲットタンパク質のバックボーンやアミノ酸側鎖を操作して、よりエネルギー的に有利な構造にするための一連の操作(例えば、振る、くねくねする、再構築する)を行うことができる。 ユーザーは、ソロリストとして、またはエボルバーとして集団で解決策に取り組むことができ、構造予測を改善すると、どちらのカテゴリーでもポイントを獲得することができる。
類似の分散コンピューティングプロジェクトとの比較
Rosetta@homeと似たような研究領域を持つ分散型計算プロジェクトがいくつかあるが、研究アプローチが異なっている。
Folding@home
タンパク質研究に関わる主要な分散コンピューティングプロジェクトの中で、BOINCプラットフォームを使用していないのはFolding@homeだけである。Rosetta@homeもFolding@homeもアルツハイマー病のようなタンパク質のミスフォールディング疾患を研究しているが、Folding@homeはそれ以上のことを専ら行っている。Folding@homeは、タンパク質がどのように折り畳まれるのか、なぜ折り畳まれるのか(あるいは、折り畳まれる可能性があるのか、そして、その後に凝集して病気を引き起こすのか)を理解するために、ほぼ独占的に全原子分子動力学モデルを使用している。言い換えれば、Folding@homeの強みはタンパク質の折り畳み過程のモデリングであり、Rosetta@homeの強みはタンパク質の設計を計算し、タンパク質の構造とドッキングを予測することである。
Rosetta@homeの結果の一部は、Folding@homeのプロジェクトの基礎として利用されている。Rosettaは最も可能性の高い構造を提供してくれるが、それが分子が取る形なのか、それとも実行可能かどうかは定かではない。 Folding@home は、Rosetta@home の結果を検証するために使用され、原子レベルの情報や、分子がどのように形を変えるかの詳細を追加で提供することができる。
この2つのプロジェクトは、計算能力とホストの多様性においても大きな違いがある。 ホストベースの中央処理装置(CPU)、グラフィックス・プロセシング・ユニット(GPU)、PS3など、平均約6,650テラフロップスの計算能力を持つFolding@homeは、Rosetta@homeの約108倍の計算能力を持っている。
World Community Grid
World Community GridのサブプロジェクトであるHuman Proteome Folding Project(HPF)の第1期、第2期ともに、Rosettaプログラムを使って様々なゲノムの構造・機能アノテーションを行っている。現在は生物学者向けのデータベース作成に利用しているが、Human Proteome Folding Projectの主任研究員であるRichard Bonneau氏は、博士号取得中にDavid Baker氏の研究室でRosettaのオリジナル開発に積極的に取り組んでいた。HPF1、HPF2とRosetta@homeの関係についての詳細は、Richard Bonneau氏のウェブサイトに掲載されている。2013年に本プロジェクトは終了した。
その他のBOINCプロジェクト
BOINC上の他のタンパク質関連の分散コンピューティングプロジェクトには、QMC@home、Docking@home、POEM@home、SIMAP、TANPAKUなどがある。Rosetta@homeアルファプロジェクトであるRALPH@homeは、Rosetta@homeに移行する前に新しいアプリケーションのバージョン、ワークユニット、アップデートをテストしている。
Predictor@homeは、Rosetta@homeと同様、タンパク質の構造予測に特化したプロジェクトである。 Rosetta@homeが構造予測にRosettaプログラムを使用していたのに対し、Predictor@homeはdTASSERの手法を使用していたが、2009年にPredictor@homeは閉鎖された。
ボランティア貢献

Rosetta@home は、研究のために個々のプロジェクトメンバーから提供された計算能力に依存している。 2020年3月28日現在、150カ国から約53,000人のユーザがRosetta@homeのアクティブなメンバーであり、約54,800台のコンピュータからのアイドルプロセッサ時間の貢献を合わせた平均性能は1.7ペタフロップスを超えている。
利用者には、その貢献度の指標としてBOINCクレジットが付与される。 各ワークユニットに付与されるクレジットは、そのワークユニットで生産されたデコイの数に、そのワークユニットのすべてのコンピュータホストが提出したデコイの平均クレジットを乗じたものである。 このカスタムシステムは、標準BOINCクライアントと最適化されたBOINCクライアントを使用しているユーザに付与されるクレジットと、Windows と Linux オペレーティングシステム上で Rosetta@home を実行しているユーザに付与されるクレジットとの間の大きな違いに対処するために設計された。CPU 作業の1秒あたりのクレジット量は、Rosetta@home の方が他のほとんどの BOINC プロジェクトよりも少ない。Rosetta@home は40以上の BOINC プロジェクトの中で13位に位置している。
CASP 実験で提出されたタンパク質の構造を予測した Rosetta@home 利用者は、その結果が科学論文で認められている。与えられたワークユニットのエネルギーが最も低い構造を予測したユーザは、「その日の予測者」(Predictor of the Day)として Rosetta@home のホームページに掲載され、メンバーであるチームと共に紹介される。また、Rosetta@home のプロフィールを作成したユーザーの中から、毎日ランダムに「その日のユーザ」(User of the Day) が選ばれ、ホームページに掲載される。
参考文献
関連項目
外部リンク
- Rosetta@home
- Ralph@home – 次期バージョンのαテスト