
チカグレロル

| |

| |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | ブリリンタ, Brilinta, Brilique |
| Drugs.com | monograph |
| MedlinePlus | a611050 |
| ライセンス | EMA:リンク、US Daily Med:リンク |
| 胎児危険度分類 |
|
| 法的規制 | |
| 投与方法 | By mouth |
| 薬物動態データ | |
| 生物学的利用能 | 36% |
| 血漿タンパク結合 | >99.7% |
| 代謝 | Liver (CYP3A4) |
| 半減期 | 7 hrs (ticagrelor), 8.5 hrs (active metabolite AR-C124910XX) |
| 排泄 | Bile duct |
| 識別 | |
|
CAS番号 |
274693-27-5 |
| ATCコード | B01AC24 (WHO) |
| PubChem | CID: 9871419 |
| IUPHAR/BPS | 1765 |
| DrugBank |
DB08816 |
| ChemSpider |
8047109 |
| UNII |
GLH0314RVC |
| KEGG |
D09017 |
| ChEMBL |
CHEMBL398435 |
| 別名 | AZD-6140 |
| 化学的データ | |
| 化学式 | C23H28F2N6O4S |
| 分子量 | 522.57 g·mol−1 |
| |
チカグレロル(Ticagrelor)は、冠動脈の血液供給に問題がある急性冠症候群の患者の脳卒中、心筋梗塞などの予防に使用される医薬品である。P2Y12受容体を拮抗阻害することにより、血小板凝集阻害薬として作用する。
欧州では2010年12月に、米国では2011年7月に、日本では2016年9月に承認されている。日本での製品名は「ブリリンタ」。
また、重篤な出血や生命に危険を及ぼす出血を対象とした解毒剤として、ベントラシマブが検討されている。
効能・効果
- 以下のリスク因子を1つ以上有する陳旧性心筋梗塞のうち、アテローム血栓症の発現リスクが特に高い場合
- 65歳以上、薬物療法を必要とする糖尿病、2回以上の心筋梗塞の既往、血管造影で確認された多枝病変を有する冠動脈疾患、末期でない慢性の腎機能障害
チカグレロルは、さまざまな患者の血栓イベント(例えば、脳卒中や心臓発作)の予防に使用される。本薬は、併用が禁忌の場合を除き、アセチルサリチル酸と併用される。PLATO試験では、急性冠症候群を発症した患者の血管性疾患による死亡、心筋梗塞、脳卒中の発症率を減少させる点で、チカグレロルがクロピドグレルに比べて優れていると結論付けられた。PLATO試験の事後サブグループ解析では、非ST上昇型の急性冠症候群患者において、チカグレロルがクロピドグレルと比較して総死亡率を低下させることが示唆された。しかし、この知見はPLATO試験の主要評価項目ではなかったため、あくまでも探索的なものと考えるべきである。後続の試験でも、チカグレロルの総死亡率の改善効果を評価するには検出力不足であった。臨床に適用するためには、チカグレロルによる総死亡率の統計的に有意な結果を得るためのさらなる研究が必要である。
チカグレロルのFDAでの適応は、急性冠症候群または心筋梗塞の既往のある患者における心血管死、心筋梗塞、脳卒中の発症率の低下である[要出典医学]。
ESC2017ガイドラインに拠ると、STセグメント上昇の有無にかかわらず急性冠症候群の患者に対しては、侵襲的、非侵襲的な初期治療戦略に拘らず、チカグレロルとアセチルサリチル酸(アスピリン)の併用による二剤抗血小板療法(DAPT)が望ましいとされているが(エビデンスレベル:IB)、経皮的冠動脈インターベンション(PCI)や血栓溶解療法の実施が計画されている場合や、その他の患者要因(例:出血リスクが高い)がある場合には、他の抗血小板剤が推奨されている。2016年ACC/AHA冠動脈疾患患者における抗血栓療法ガイドラインでは、エビデンスレベルは低い(IIaB)ものの、同様の推奨がなされている。さらに、2017年のESC 二剤抗血小板療法継続ガイドラインでは、経皮的冠動脈インターベンションを受ける安定した冠動脈疾患の患者に対して、血栓症や出血リスクを考慮した上で、医師がチカグレロルを投与することを認めている。
心臓塞栓症を伴わない軽度の虚血性脳卒中または高リスクの一過性脳虚血発作(TIA)患者において、チカグレロル単剤療法は、アスピリンと比較して、脳卒中、心筋梗塞、死亡の複合項目の減少において、数値的には減少したものの統計的には有意ではなかった。大規模なTHALES無作為化比較試験では、チカグレロルとアスピリンの併用療法は、アスピリン単独療法に比べて、30日後の脳卒中または死亡の複合項目を減少させる点で優れていたが、重度の出血のリスクが増加した。軽度の虚血性脳卒中やハイリスクのTIA後の短期的な二剤抗血小板療法の役割は支持されているが、現在の処、このコホートにおけるチカグレロル+アスピリンと現在の標準治療であるクロピドグレル+アスピリンとの直接比較は発表されていない。脳卒中後の臨床におけるチカグレロルの役割を明確にするためには、この点に関するさらなる研究(現在進行中のCHANCE-2試験の結果を含む)が必要である。軽度の虚血性脳卒中または高リスクのTIAに対するチカグレロル単剤療法およびチカグレロルとアスピリンの併用療法とアスピリン単剤療法を比較した試験では、頭蓋内または頭蓋外の動脈に同側の狭窄がある患者のサブグループは、同側の狭窄がないサブグループに比べて脳卒中再発の絶対リスクが高く、絶対的なベネフィットの大きさも大きかった。しかし、これらのサブグループ解析は、仮説を立てるだけの役割に留まった。
急性冠症候群患者を対象としたチカグレロルとクロピドグレルの比較試験(PLATO試験)では、チカグレロルを投与された患者は、感染症による死亡リスクが低いことが示された。チカグレロルによるTargeting Platelet-Leukocyte Aggregates in Pneumonia With Ticagrelor(XANTHIPPE)試験では、肺炎で入院した患者にチカグレロルを投与した処、肺機能の改善が認められた。
禁忌
チカグレロルは、以下の患者に禁忌である。
- 出血している患者(頭蓋内出血、消化管出血、尿路出血、喀血、硝子体出血など)
- 血友病の患者
- 頭蓋内出血の既往歴のある患者
- 中等度または重度の肝障害のある患者
- 本剤の成分に対し過敏症の既往歴のある患者
- 強いCYP3A阻害剤(イトラコナゾール、ボリコナゾール、クラリスロマイシン、ネルフィナビル、リトナビル、コビシスタットを含む薬剤)を投与中の患者
- 強いCYP3A誘導剤(リファンピシン、リファブチン、カルバマゼピン、フェノバルビタール、フェニトイン、セイヨウオトギリソウ含有食品)を投与中の患者
副作用
重大な副作用は、以下の3つである。
- 出血
- 脳出血などの頭蓋内出血(初期症状:頭痛、悪心・嘔吐、意識障害、片麻痺など、1%)、
- 消化器系出血(歯肉出血、直腸出血、出血性胃潰瘍など、3.6%)など
- アナフィラキシー
- 血管浮腫
一般的な副作用は、出血のリスクの増加(重篤な場合もある)と息切れ(呼吸困難)である。呼吸困難は通常一過性で、重症度は軽度から中等度であるが、フォローアップの1カ月未満、1~6カ月、6カ月以上の期間では、クロピドグレルと比較してリスクが高くなる。治療を中止することはまれであるが、持続しない患者や治療法を変更する患者もいる。しかし、チカグレロルは急性冠症候群(ACS)での有効性と安全性に影響を与えないため、患者は安心して治療を続けるべきである。さらに、ベースラインのACS、心不全、重大な肺疾患を持たない患者において、呼吸困難と心機能および肺機能の有害な変化との間に関連性はない。
ACS患者において、治療開始後1週間で3秒以上の心室休止が発生する可能性があるが、ほとんどが無症状で一過性のものであり、臨床的な徐脈性有害事象の増加を引き起こすことはないと考えられる。進行した洞房結節疾患のある患者にチカグレロルを使用する場合は注意が必要である。発疹や痒みなどのアレルギー性皮膚反応は1%未満の患者にしか認められていない。
相互作用
ケトコナゾールやグレープフルーツジュースなどの肝酵素CYP3A4の阻害剤は、チカグレロルの血漿中濃度を上昇させ、その結果、出血などの副作用を引き起こす可能性がある。チカグレロルは弱いCYP3A4阻害剤であり、CYP3A4で代謝される薬剤の濃度を上昇させることが知られている。しかし、推奨用量のアトルバスタチンおよびシンバスタチンでは、この相互作用は臨床的には重要ではないと考えられる。CYP3A4誘導剤、例えばリファンピシンやセイヨウオトギリソウなどはチカグレロルの効果を低下させる可能性がある。CYP2C9を介した相互作用の証拠はない。
また、チカグレロルはP糖タンパク質(P-gp)を阻害するため、ジゴキシン、シクロスポリンなどのP-gp基質の血漿中濃度が上昇します。チカグレロおよびAR-C124910XX(O-脱エチル化によって生成されるチカグレロの活性代謝物)のレベルは、P-gp阻害剤によって有意な影響を受けない。
二剤抗血小板療法(DAPT)として、低用量アスピリン(1日75~100mg)とチカグレロルを併用することが推奨されている。チカグレロルと100mg/日以上のアスピリンの併用は効果が低い可能性がある。
作用機序
チエノピリジン系のプラスグレル、クロピドグレル、チクロピジンと同様に、チカグレロルはP2Y12サブタイプのアデノシン二リン酸(ADP)受容体を遮断する。他の抗血小板薬とは異なり、チカグレロルはADPとは異なる結合部位を持つアロステリック・アンタゴニストであり、その遮断は可逆的である。さらに、本剤は肝臓での活性化を必要としないため、CYP2C19酵素に関する遺伝子変異を有する患者にも有効である可能性がある(ただし、クロピドグレルがこのような遺伝子変異の影響を大きく受けるかどうかは定かではない)。
薬物動態
チカグレロルは腸から速やかに吸収され、バイオアベイラビリティーは36%で、約1.5時間後にピーク濃度に達する。主な代謝物であるAR-C124910XXは、CYP3A4を介してシクロペンタン環の5位で脱ヒドロキシエチル化されて速やかに生成される。この代謝物は約2.5時間後にピークを迎える。チカグレロルとAR-C124910XXは、ともに血漿タンパク質に結合し(99.7%以上)、薬理活性を有している。血漿中濃度は、1260mg(1日投与量の7倍量)までは投与量に線形に依存する。代謝物はチカグレロールの血漿中濃度の30~40%に達する。薬物および代謝物は主に胆汁および糞を介して排泄される。
チカグレロルの血漿中濃度は、高齢者、女性、アジア系民族、軽度の肝機能障害を有する患者で僅かに上昇(12~23%)した。また、「黒人」を自認する患者および重度の腎機能障害を有する患者では、血漿中濃度が低下した。これらの差は臨床的には重要ではないと考えられる。日本人では、白人に比べて40%、体重補正後では20%濃度が高くなる。なお、重度の肝機能障害を有する患者を対象とした試験は行われていない。
チカグレロルは、その可逆的な作用機序により、クロピドグレルよりも早く、短く作用することが知られている。そのため、1日1回ではなく2回服用しなければならず、服薬コンプライアンスの面で不利になるが、効果が迅速に回復するため、手術前や副作用が発生した場合には有効である。
化学的特徴
シクロペンタン環は糖のリボースに似ており、窒素を多く含む芳香環系は核酸塩基のプリンに似ていることから、分子全体がアデノシンに類似している。この物質は、バイオ医薬品分類システムの下で、低溶解性かつ低膜透過性に分類される。
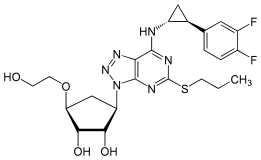
ヌクレオシドアナログのチカグレロル
|

ヌクレオシドの1つアデノシン
|
類薬との比較
クロピドグレル
PLATO試験では、急性冠症候群の患者の治療において、チカグレロルはクロピドグレルよりも死亡率が良好であった(9.8%対11.7%、p<0.001)。チカグレロルを投与された患者は、血管系の原因、心臓発作、脳卒中による死亡率は低かったものの、非致死的出血の可能性が高く(16.1%対14.6%、p=0.0084)、冠動脈バイパスグラフト術に関係しない大出血の発生率も高かった(4.5%対3.8%、p=0.03)。致命的な頭蓋内出血の発生件数はチカグレロル投与群で多かったものの、致命的な非頭蓋内出血の発生件数は有意に少なく、致命的または生命を脅かす出血に対する全体的な効果はクロピドグレル投与群と比較して中立的であった(p=0.70)。大出血の発生率には差がなかった。有害事象による試験薬の中止は、チカグレロルでクロピドグレルよりも多く発生した(7.4%対6.0%、p<0.001)。
PLATO試験では、総患者数18,624人のうち1,800人を占める米国の患者において、チカグレロル投与群に、クロピドグレル投与群と較べて統計的に有意ではない転帰の悪化傾向が認められた。また、複合エンドポイントである心血管系(死亡、心筋梗塞、脳卒中)については、チカグレロル投与群で12.6%、クロピドグレル投与群で10.1%と、ハザード比が逆転した(HR = 1.27)。この結果は、米国ではアスピリン維持量が高いという違いによるものではないかという意見がある。また、中央判定委員会は、クロピドグレル(比較対照)群で心筋梗塞が45件余分に認められたが、チカグレロル群では全く認められなかったため、チカグレロルの心筋梗塞アウトカムが改善されたという意見もある。このような裁定がなければ、試験の主要な有効性の結果は有意ではないはずである。
また、アジア人患者におけるチカグレロルの有効性と安全性についても意見が分かれている。前述したように、チカグレロルは血栓症に大きな効果をもたらすが、同時に出血リスクも増加する。特にアジア人は出血イベントを起こしやすいことが知られているため、きわめて重要な意味を持っている。このような脆弱な集団におけるチカグレロルのリスク/ベネフィット比に関する最新のエビデンスは、やや議論の余地がある。無作為化比較試験(RCT)のいくつかのメタアナリシスでは、アジア人患者において、チカグレロルは重篤な出血性イベントの増加と関連しており、虚血性疾患に関する利点は伴っていないことが示唆されている。しかし、これらのメタアナリシスは、主にサンプルサイズが比較的小さい2つのRCTの結果にもとづいており、デザイン上の落とし穴があったため、アジア人全体に一般化することはできない。一方、最近の観察研究のメタアナリシスでは、チカグレロルが大出血の有意な増加を伴わずに虚血性疾患でのベネフィット(主に脳卒中のリスクを減少させる)をもたらすことが示唆されている。今回の研究は、「リアルワールド」の環境下で行われたことから、強い支持を得ているが、臨床現場での明確な推奨事項を示すためには、さらなる質の高い研究が不可欠である。
プラスグレル
2019年には、急性冠症候群の患者を対象にチカグレロルとプラスグレルを比較したISAR-REACT 5試験の結果が発表された。ST上昇を伴うまたは伴わない急性冠症候群を呈した患者では、死亡(4.5%対3.7%)、心筋梗塞(4.8%対3.0%)、または脳卒中(1.1%対1.0%)の発生率は、チカグレロルを投与された患者よりもプラスグレルを投与された患者で有意に低く(総計:9.3%対6.9%;ハザード比1.36;95%信頼区間1.09〜 1.70;P = 0.006)、大出血の発生率は有意ではなかった(5.4%対4.8%;ハザード比1.12;95%CI0.83〜1.51;P = 0.46)。
研究開発
JAMA Cardiology誌に掲載された最近のin vitro 試験およびマウスモデルによる研究では、メチシリン耐性黄色ブドウ球菌(MRSA)やバンコマイシン耐性腸球菌(VRE)などの抗生物質耐性グラム陽性菌に対する抗菌性が示された。重要な点は、この研究では、急性冠症候群(ACS)後の標準的な投与量をはるかに上回る殺菌作用を持つチカグレロルの濃度を使用したことである。ある後ろ向きコホート研究では、「ACSに対して従来の用量のチカグレロルを投与した患者では、チカグレロル投与後1年間のグラム陽性感染症のリスクがクロピドグレルと比較して64%減少した。また、デンマークの観察コホート研究では、チカグレロル治療を受けた患者の黄色ブドウ球菌による菌血症の1年間のリスクが、クロピドグレルと比較して低いことが判明した。これらの知見は試験デザインによって制限されているが、チカグレロルの抗生物質としての実用性を評価するためには、ヒトでの無作為化試験をさらに行う必要がある」とされている。
参考資料
外部リンク
- “Ticagrelor”. Drug Information Portal. U.S. National Library of Medicine. 2021年6月12日閲覧。