
Covaxin
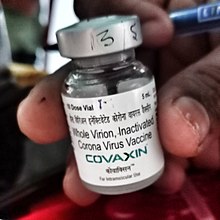 Covaxinワクチンのバイアル
| |
| ワクチン概要 | |
|---|---|
| 病気 | SARSコロナウイルス2 (SARS-CoV-2) |
| 種別 | 不活化ワクチン |
| 臨床データ | |
| 販売名 | Covaxin |
| 法的規制 |
|
| 投与方法 | 筋肉内注射 |
| 識別 | |
| ATCコード | None |
| DrugBank | DB15847 |
Covaxin(コバクシン)は、インドで開発されたCOVID-19ワクチンの一種。BBV152とも呼ばれ、インドに本拠地を置くバーラト・バイオテック社がインド医学研究評議会と共同で開発した、不活化ウイルスベースのワクチンである。
インド国内で接種されているほか使用を認めた各国へ輸出され、いわゆる「ワクチン外交」にも利用されている。世界保健機関(WHO)は2021年11月3日に緊急使用を承認し、低価格なうえに2 - 8℃で長期保管できることから低所得層への接種にも適しているとの見解を示している。
臨床研究
第I相および第II相試験
2020年5月、インド医学研究評議会(ICMR)の国立ウイルス学研究所は、COVID-19ワクチンを完全に独自開発するためのウイルス株を承認し、提供した。2020年6月、同社は、インド政府の医薬品規制当局(DCGI)から、Covaxinという名称の開発用COVID-19ワクチンの第I相および第II相ヒト臨床試験を実施する許可を取得した。ワクチン候補の第I相および第II相の無作為化二重盲検法・プラセボ対照臨床試験のため、インド医学研究評議会により合計12施設が選定された。
2020年12月、同社は第I相試験の報告書を発表し、medRxivプレプリントを通じて結果を発表した。後に『ランセット』誌に掲載された。
第III相試験
2020年11月、コバクシンは、第I相および第II相試験の完了後、第III相のヒト臨床試験を実施するための承認を取得した。この試験は、18歳以上のボランティアを対象とした無作為化二重盲検法・プラセボ対照試験が含まれ、11月25日に開始された。第III相試験では、インド全土から約26,000人のボランティアが参加した。第III相試験は、デリー、カルナータカ州、西ベンガル州などインド国内の複数の州からなる、合計22施設で実施された。第III相試験の拒絶率は、第I相および第II相試験よりもはるかに高かった。その結果、12月22日までに募集したボランティアは13,000人にとどまり、1月5日までに23,000人に増加した。
2021年3月現在、第III相試験の中間有効率は81%である。なお、第2次中間分析と最終分析の全てのデータは、査読付きジャーナルを通じてまだ公開されていない。
アルファ変異株(系統 B.1.1.7/英国)
2020年12月、英国では新たなSARSコロナウイルス2の変異株である系統 B.1.1.7が同定された。この変異株に関する研究が行われ、bioRxivで発表された予備的な結果では、コバクシンがこのウイルス株を中和するのに有効であることが示された。
製造
このワクチン候補は、バーラト・バイオテック社の社内ベロ細胞製造プラットフォームで製造され、約3億用量を供給する能力を持っている。同社は現在、コバクシンを製造するために、ハイデラバードのゲノムバレー施設に第2工場を設置中である。同社は、ワクチンを製造するための国内の別の場所のために、オリッサ州のような他の州政府と協議中である。この他にも、コバクシン製造のためのグローバルな提携も模索している。
2020年12月、オキュゲン社がバーラト・バイオテックと提携し、米国市場向けにコバクシンを共同開発した。2021年1月、Precisa Med社がバーラト・バイオテックとブラジルでのコバクシン供給契約を締結した。
緊急使用許可
2020年12月、バーラト・バイオテック社は、インド政府の医薬品規制当局(DCGI)に緊急使用許可(EUA)を申請した。緊急使用承認を申請したのは、セラム・インスティテュート・オブ・インディア、ファイザー社に次いで3社目である。
2021年1月2日、中央医薬品標準管理機構(CDSCO)がEUAの承認を勧告し、1月3日に承認された。緊急承認は、第III相試験のデータが公表される前に行われた。このことは一部のメディアで批判された。
2021年11月3日、WHOが緊急使用を承認した。
外部リンク
- Covaxin(英語) - Bharat Biotech
- “How Bharat Biotech's Covaxin Vaccine Works”. The New York Times. 2021年3月8日閲覧。(英語)
|
新型コロナウイルス感染症 (COVID-19)
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| SARSコロナウイルス2 |
|
||||||||||||||||||
| 治療 |
|
||||||||||||||||||
| 感染拡大 | |||||||||||||||||||
| 影響 (コロナ禍) |
|
||||||||||||||||||
| 社会の対応 |
|
||||||||||||||||||
| 組織 |
|
||||||||||||||||||
| その他関連項目 | |||||||||||||||||||