COVID-19ワクチン
COVID-19ワクチン(コビッド19ワクチン、英: COVID-19 vaccine)は、新型コロナウイルス感染症(COVID-19)の原因ウイルスであるSARSコロナウイルス2(SARS-CoV-2)に対して、ヒトに獲得免疫を提供することを目的としたワクチンである。新型コロナウイルスワクチン、新型コロナワクチンとも呼ばれる。
2021年5月時点で、接種開始済みから開発中まで、複数の方式や製造元のワクチンが存在する(mRNAワクチン、DNAワクチン、ウイルスベクターワクチン、不活化ワクチン、組換えタンパクワクチン、ペプチドワクチンなど)。
世界的に見て、2020年末や2021年初頭から複数の製薬企業が開発・製造した複数種のCOVID-19ワクチンの接種が始まっている。各国のワクチンの接種状況を概観すると、早期にワクチン調達契約を結ぶことに成功して既に大規模に接種が行われた国がある一方、ワクチン調達で遅れをとり接種がほとんど進んでいない国も存在する(後節の「ワクチンの確保・接種状況」を参照)。オーストリアのように接種の義務化を決定した国もある。
概要

既に複数の製薬企業によってワクチンは臨床試験も済んでおり、世界各地で接種は行われている。有効性は各ワクチンごとに異なる(後節の「有効性」を参照)。
各国・各地の接種状況については後節の「ワクチンの確保・接種状況」を参照のこと。
いまだにワクチン開発に成功していない製薬会社の中には、今も新たな種類のCOVID-19ワクチンの開発の努力を続けている企業もある。なお2021年5月18日時点で、日本の製薬企業はいずれも自社のCOVID-19ワクチンの承認を得ることに成功していない。
開発開始までの経緯と開発の加速
COVID-19の大流行に先立ち、重症急性呼吸器症候群(SARS)や中東呼吸器症候群(MERS)などの病気を引き起こすコロナウイルスの構造と機能に関する知識が確立されていた為、2020年初頭に様々なワクチン技術の開発を加速できた、とされた。2020年1月10日、SARS-CoV-2の遺伝子配列データがGISAIDを通じて共有され、同年3月19日までに、世界の製薬業界がCOVID-19への取り組みを大々的に発表した。
2020年代に入り、COVID-19は世界規模で急ピッチに広がりを見せたことから、各国の研究機関や医薬品メーカーは、新たなワクチンの開発や他のウイルス用に開発された既存ワクチンの再評価に乗り出した。世界保健機関(WHO)は、2020年5月までに世界で118の計画が進行中とするリストを公表。うち8の計画は、その時点で既に欧米や中華人民共和国(中国)で臨床試験の段階に入っていた。また、WHOはワクチン開発に各国が共同出資・購入する枠組み「COVAX(コバックス)」を立ち上げた。
なお、2020年6月時点では、「最初に開発されるワクチンについては、感染防止よりも重症化や死亡を防ぐタイプのワクチンを開発する可能性がある」などと報道されていた。また、高齢者にはワクチンが効きにくいと指摘する声もあった。
COVID-19用ワクチンの製造に当たり、新たな製造手法を模索する企業も現れた。これは、従来の鶏卵によるインフルエンザワクチンの生産手法を応用した場合、生産性が低いうえに時間がかかるというリスクがあること、また、卵に注入したウイルスが変異して、ワクチンの有効性が低下することも考えられるためである。具体的には、DNAワクチンやmRNAワクチンの開発が進められることとなった。
2020年5月時点で、WHO、感染症流行対策イノベーション連合(Coalition for Epidemic Preparedness Innovations, CEPI)、およびゲイツ財団(GF)は、COVID-19感染症の継続を防ぐためにいくつかのワクチンが必要になるという見通しのため、資金と組織のリソースを投入していた。ワクチン候補の迅速な投資と開発のために20億ドルの世界基金を組織しているCEPI は、2020年9月に、ライセンス取得を支援するための臨床データが同年末までに入手できる可能性があることを示した。2020年5月4日には、WHOが主催したテレソン(長時間特別番組)で、40カ国から81億ドルの誓約書が寄せられた。同時に、WHOは、第II/III相臨床試験に到達した複数のワクチン候補の同時評価のための国際的な「連帯試験」の展開も発表した。
2020年11月、バーレーンは中国のシノファーム社製ワクチンの緊急販売承認を与え、アラブ首長国連邦(UAE)がこれに続いた。12月には、バーレーンと英国が米ファイザー社製ワクチンを緊急時の使用を承認した一方、UAEとカナダは一般使用を承認した。
臨床試験の状況
第III相臨床試験では、いくつかのCOVID-19ワクチンが、症候性COVID-19感染症の予防に95%という高い有効性を示している。2021年4月現在、16種のワクチンが少なくとも1つの国の規制当局から一般公衆用として認可を受けている。2種類のRNAワクチン(ファイザー-バイオンテック社製ワクチン、モデルナ社製ワクチン)、7種類の従来型不活化ワクチン(BBIBP-CorV、CoronaVac、Covaxin、WIBP-CorV、CoviVac、Minhai-Kangtai、QazVac)、5種類のウイルスベクターワクチン(スプートニク・ライト、スプートニクV、オックスフォード-アストラゼネカ、コンビディシア、ジョンソン・エンド・ジョンソン)、2種類のタンパク質サブユニットワクチン(EpiVacCorona、RBD-Dimer)である。合計すると、2021年3月時点で、308のワクチン候補が様々な段階で開発されており、73件が臨床研究中で、そのうち24が第I相試験、33が第I/II相試験、16が第III相試験となっている。
生産・配布計画
多くの国では、高齢者などの合併症のリスクが最も高い人や、医療従事者などのウイルスへの曝露・感染のリスクが高い人を優先して段階的に配布する計画が実施されている。また、ワクチンの入手性が向上するまでの間、できるだけ多くの人々に接種を拡大するために、単回接種による暫定使用が検討されている。2021年5月19日時点、各国の保健機関からの公式報告によると、全世界で13億回のCOVID-19ワクチンが投与された。アストラゼネカ-オックスフォードは2021年に30億回、ファイザー-バイオンテック社13億回、スプートニクV、シノファーム、シノバック、ジョンソン・エンド・ジョンソン社はそれぞれ10億回の生産を見込んでいる。モデルナは2021年に6億回、コンビディシアは5億回の投与を目標としている。2020年12月までに100億回以上のワクチンが各国から予約注文されており、世界人口の14%を占める高所得国がその約半数を購入している。
欧米企業のワクチンを十分に調達する経済力がない中・低所得国に対しては中華人民共和国やロシア連邦、インドが大量のワクチンを輸出しており、外交的影響力を拡大する意図が指摘されている。日本政府は購入したアストラゼネカ製ワクチンを、台湾やベトナム、インドネシア、タイ、フィリピン、マレーシア、ブルネイへ無償提供している。
接種状況
既に世界各地でワクチンの接種が開始されている。日本含む各国・各地の接種状況については後節の「ワクチンの確保・接種状況」を参照のこと。
接種を行った人々に様々なインセンティブ(優遇)・特典を与えて接種を加速させる取り組み や、接種済みであることを証明する「ワクチンパスポート」を発行する動きもある。ガイダンスによると、完全に予防接種を受けた人は、マスクなしで、また物理的な距離を置くことなく、屋内と屋外のすべての活動に参加できるようになった。しかし、2021年7月、アメリカ疾病予防管理センターは、完全にワクチン接種された人を含むすべての人に、ウイルスの感染がかなりまたは多い地域の公共の屋内の場所でマスクを着用するように勧告した。
ワクチンの余剰・廃棄問題
ワクチンの開発・生産が進んで供給量が増えたことや、接種への忌避感が根強い地域があることなどで、ワクチンおよびその生産能力の余剰と、使用期限切れによる廃棄が生じている。先進国のほか、南アフリカ共和国で製薬会社アスペンが他のアフリカ諸国への供給用に建設したワクチン工場は、アフリカ諸国の接種率が低いにもかかわらず2022年6月時点で受注が得られず閉鎖危機にある。
沿革
SARSとMERSのワクチン開発
2003年時点、鳥類感染性気管支炎ウイルス (infectious bronchitis virus) 、犬コロナウイルス、猫コロナウイルスなど、コロナウイルスによって引き起こされるいくつかの動物の病気に対してワクチンは製造されていた。ヒトに影響を与えるコロナウイルス科のウイルスに対するワクチンを開発するための以前のプロジェクトは、重症急性呼吸器症候群(SARS)と中東呼吸器症候群(MERS)を対象としていた。SARS およびMERS に対するワクチンは、ヒト以外の動物でテストされている。
2005年と2006年に発表された研究によると、SARSを治療するための新しいワクチンと医薬品の特定と開発は、当時の世界中の政府と衛生行政機関にとって優先事項だった。2020年の時点で、ヒトのSARSに対して安全で効果的であることが証明されている治療法や予防ワクチンは無い。
MERSに対し確立されたワクチンも存在しない。MERSが普及したとき、既存のSARS研究は、MERS-CoV感染に対するワクチンと治療法を開発するための有用なテンプレートを提供する可能性があると考えられていた。2020年3月現在、ヒトでの第I相臨床試験を完了した(DNAベースの)MERSワクチンが1種、その他3種のワクチンが進行中であり、いずれもアデノウイルスベクター型2種(ChAdOx1-MERS、BVRS-GamVac)、MVAベクター型1種(MVA-MERS-S)である。
2020年のCOVID-19ワクチン開発

COVID-19が世界的に蔓延し始めた2019年末 - 2020年初頭の時点では、ヒトのコロナウイルス感染を予防するためのワクチンは存在していなかった。2019年12月にCOVID-19コロナウイルスが検出された後、COVID-19の遺伝子配列が2020年1月11日に公開され、発生に備えて予防ワクチンの開発を早めるための緊急の国際的対応が引き起こされた。
2020年2月時点では、世界保健機関(WHO)は、原因ウイルスであるSARSコロナウイルス2(SARS-CoV-2)に対するワクチンが18カ月以内に利用可能になるとは予想していないと述べていた。2020年初頭に世界的にCOVID-19の感染率が急増したことで、国際的なアライアンスや政府の取り組みが刺激され、複数のワクチンを短期間で製造するためのリソースを緊急に整理し、3月には4つのワクチン候補がヒト評価に入ることとなった(後節の「2020年に開始された臨床試験」の表を参照)。
2020年4月、WHOは、異なる技術と流通を持つ3種類以上のワクチンを開発するための総費用を80億米ドルと見積もった。2020年4月までに、「19カ国のほぼ80の企業や研究機関」がこの仮想的なゴールドラッシュに取り組んでいた。また、4月には、CEPIは、COVID-19に対するワクチン候補のうち、6つのワクチンが国際的な連合によって第II-III相試験を経て開発のために選ばれ、3つのワクチンは最終的なライセンス取得に向けて規制と品質保証を経て合理化されなければならないと見積もっている。別の分析によると、10のワクチン候補が同時に初期開発を必要とし、そのうちのいくつかがライセンス取得に向けた最終的な道筋として選ばれる前に、10のワクチン候補が同時に初期開発を必要とすると見積もっている。
2020年7月、英国国家サイバーセキュリティ―センター (National Cyber Security Centre) として、それぞれの政府および軍隊の英米諜報機関およびセキュリティ組織が、カナダ通信保安局 (Communications Security Establishment) 、アメリカ合衆国国土安全保障省国家保護・プログラム総局 (Cybersecurity Infrastructure Security Agency) 、アメリカ国家安全保障局(NSA)は、ロシアの国家支援ハッカーが他の国の学術機関や製薬機関からCOVID‑19治療とワクチン研究を盗もうとした可能性があると主張した。ロシアはそれを否定した。
開発状況
2020年の間に、年初からのCOVID-19ワクチン開発の取り組み全体の大きな変化は、多国籍製薬業界と各国政府との共同研究の増加と、COVID-19ワクチンに注力する多くの国のバイオテクノロジー企業の多様性と増加である。CEPIによると、COVID-19ワクチン開発の一般的な地理的分布は、北米の組織が世界のCOVID-19ワクチン研究の約40%を占めているのに対し、アジアとオーストラリアでは30%、ヨーロッパでは26%、南米とアフリカではいくつかのプロジェクトが存在している。
ワクチン開発がスタートすると分散コンピューティングプロジェクトのFolding@homeへの関心が高まったことで、2020年3月下旬には演算能力は約1.22 EFLOPS、2020年4月中旬には約2.43 EFLOPSを達成し、世界初のエクサフロップ・コンピューティング・システムとなり、TOP500の全スーパーコンピュータの合算を上回る能力を獲得した。
国際機関
ワクチン開発を加速させ、流通に備えるための国際的な提携を形成している組織があるが、その中には、2020年5月初旬に81億米ドルの資金調達を開始し、史上前例のない規模で協力、研究の加速化、国際的なコミュニケーションを促進している世界保健機関(WHO)も含まれている。WHOはまた、世界的なワクチン開発を調整するためのCovid-19 Vaccines Global Access(COVAX)を実施し、GAVIやCEPIと共同で Access to COVID-19 Tools (ACT) Accelerator のワクチンの柱となっている。7月、WHOは、世界人口の最大60%を占める165カ国が、最終的な認可ワクチンの公正かつ衡平な配分のためのWHO COVAX計画に合意したことを発表した。COVAXは、COVID-19ワクチンの開発と製造を加速し、「認可ワクチンへのアクセスが全ての国に公平に提供されること」を保証することを目標としている。具体的には2021年末までに、各参加国が最前線の医療従事者やリスクの高い人々を保護し、最も脆弱な20%の人口にワクチンを接種する ために、保証された分量を受け取る(最大20億回分を平等に提供する)ことを保証する。
CEPIは、国際保健当局およびワクチン開発者と協力して、さらに20億米ドルの基金を創設。公的、私的、慈善団体、市民社会の組織間のグローバルパートナーシップで、8つのワクチン候補の研究と臨床試験を加速するために資金を提供し、当面(2020年〜2021年)は、ライセンスの完全な開発のためにいくつかの候補を支援することを目標としている。英国、カナダ、ベルギー、ノルウェー、スイス、ドイツ、オランダは既に9億1500万米ドルを寄付しており、ワクチンの研究と配布を専門とする民間の慈善団体であるビル&メリンダゲイツ財団(ゲイツ財団)は、2億5000万米ドルを寄付している。
2020年6月4日、英国のロンドンから、G7およびG20諸国の35の国家元首を含む、52カ国の民間および政府の代表者の間で仮想サミットが調整され、88億米ドルが調達された。ワクチンと予防接種のためのグローバルアライアンス(GAVI)により、2025年までに発展途上国の3億人の子供たちがワクチンを摂取できるよう準備する。主な寄付はゲイツ財団からの16億米ドル と英国政府による5年間で年間3億3000万ポンド(2020年6月には約21億米ドル)など。
2020年12月時点では、ACTアクセラレーターにより24億米ドルが調達されており、9つのワクチン候補がCOVAXとCEPIによって資金提供され、189カ国が最終的なワクチンの展開計画に取り組んでいる。
感染症流行対策イノベーション連合 (CEPI)
感染症流行対策イノベーション連合はノルウェー政府、インド政府、ビル&メリンダ・ゲイツ財団、および公益信託団体ウェルカム・トラストの出資によって2017年に世界経済フォーラム(ダボス会議)にて発足した、公的機関、民間機関、慈善団体および市民団体の間でのグローバルな協働体である。日本の厚生労働省も創設に関わり2017年より拠出を行ってきた。
2020年1月23日、CEPIは以下3研究チームがワクチン開発に向けた作業を開始し、少なくとも1種類のワクチンの臨床試験を6月までに開始すると発表した。また、夏にも人へ臨床試験を行い、ワクチン承認は早ければ年内になるとも述べた。
- 米医薬品・ワクチン開発のモデルナ (Moderna, Inc.)(英語) (MRNA.O) とアメリカ国立アレルギー・感染症研究所 (NIAID) の連携
- 製薬会社 イノビオ・ファーマシューティカルズ (Inovio Pharmaceuticals, Inc.) (INO.O)
- 豪クイーンズランド大学のチーム
この他、米Vir Biotechnology社もワクチン開発計画に加わり、SARSやMERSの生存者から同定されたモノクローナル抗体(mAbs)が本ウイルスに有効かどうか調べる。
イノビオはMERSの最も先進的なワクチン候補 INO-4700をもっており、ウイルスのDNA塩基配列が公表されて3時間以内にウイルスをデザインできた。CEPIから最大900万ドル(約9億8000万円)の助成金を受け、2020年初夏にも中東・アフリカ現地での第II相臨床試験に入る予定 で、大規模な臨床試験は年末までに中国で行いたいという。
2月3日、英グラクソ・スミスクライン (GSK) はパンデミックワクチンで確立されたアジュバント(抗原性補強剤)の基盤技術を提供するためにCEPIの協働に参加すると発表した。
2月25日、モデルナは開発中のCOVID-19のワクチンを、ヒトに投与する安全性試験(第I相試験)向けに米国立アレルギー感染症研究所 (NIAID) に出荷した。ヒトへの臨床試験は2カ月以内の開始を見込むが、一般に入手できるようになるには1年半かかる可能性があるという。
日本
2020年3月12日、田辺三菱製薬は、カナダの子会社が製造する植物由来の粒子を利用し、ワクチン開発に着手すると発表した(CoVLP)。
2020年3月5日、大阪大学発の創薬企業アンジェスは、DNAプラスミド技術を活かしたDNAワクチンを大阪大学と共同で開発し、タカラバイオが製造すると発表した。同年6月30日より治験を開始し、7月末までに30人を対象に実施する。
2020年5月7日、塩野義製薬は、子会社のUMNファーマが国立感染症研究所と共同で、年内の臨床試験開始を目指していることを公表した。最短で2020年内の臨床試験開始を予定している。市場への投入は2021年秋になる見込みで、同年末までに3,000万人分の生産を目標とする。
第一三共、東京大学医科学研究所は、最短で2021年3月からワクチンの臨床試験を開始することを目指すと報道された。
2020年6月27日、九州大学は、九州大学発のベンチャー企業であるKAICOと共同で、新型コロナウイルスのワクチン候補となるたんぱく質の開発に成功したと発表した。2021年からワクチンの臨床試験開始を目指している。
2020年8月時点でワクチンの開発が急がれた一方、(その時点では)専門家からは「感染そのものを予防する効果は証明が難しい」という懸念が出た。また、東京大学医科学研究所の石井健教授は「(ワクチン開発を)急げば急ぐほど安全性の担保はおろそかになる」と訴えている。この懸念に対し、米国国立研究機関博士研究員でウイルス学、免疫学を専門とする峰宗太郎医は「動物実験などの結果を踏まえると、『(感染予防効果は)あると考えてよい』と思います」 と述べている。
日本国内でも「臨床試験の段階で発熱などの副作用が発生しているケースも見られる」とか、2020年12月20日時点で「ファイザー/バイオンテックのワクチンは、27万人への接種で6人(100万人あたり22人)のアナフィラキシーが報告されている」とか、2020年1月23日の報道では「モデルナのワクチンは、400万人の接種でアナフィラキシーが起きたのは10人(100万人あたり2.5人)であり、いずれの患者もその後回復した」と報道された。
日本では2020年12月18日にファイザーが厚生労働省に承認申請を行ったほか、国内メーカや大学などで実用化を目指して開発が行われているが、いずれも2021年に臨床試験を開始する目標であり、まだ実用化はされていない、とされた。
2021年2月5日、アストラゼネカが厚生労働省に承認申請を行った。
2021年2月12日、ファイザー製のコロナワクチン「コミナティ」の特例承認が了承され、2021年2月14日に正式に特例承認された。なお、当該ワクチンの法令上の名称は「コロナウイルス修飾ウリジンRNAワクチン(SARS-CoV-2)」である。
2021年3月5日、モデルナのワクチンについて、日本での窓口企業の武田薬品工業が厚生労働省に承認申請を行った。
2021年5月20日、アストラゼネカのコロナワクチンである「バキスゼブリア」とモデルナのコロナワクチンである「COVID-19ワクチンモデルナ」(後に「スパイクバックス」へ名称変更)の特例承認が了承され、2021年5月21日に正式に特例承認された。なお、アストラゼネカのウイルスベクターワクチンについての法令上の名称は「コロナウイルス(SARS-CoV-2)ワクチン(遺伝子組換えサルアデノウイルスベクター)」である。ただ、モデルナのワクチンについてはファイザーに続いて公的接種の対象とされたものの(後述する大規模会場で使用されている)、アストラゼネカのワクチンについては、諸外国で副反応と見られる血栓症の発生があったことから、薬事承認はされたものの公的接種の対象外とされた。その後、同年8月3日に原則40歳以上を対象に公的接種の対象に追加された。
2021年5月24日、ジョンソン・エンド・ジョンソンのワクチンについて、傘下のヤンセンファーマが厚生労働省に承認申請を行った。2022年5月30日、厚生労働省の専門部会はジョンソン・エンド・ジョンソンのワクチン「ジェコビデン」について製造販売を承認することを了承した。その後、同年6月20日に厚生労働省は「ジェコビデン」の製造販売を承認した。ただし、当該ワクチンに関しては、厚生労働省は予防接種法上の公費負担で打てるワクチンに含めない方針を示しており、希望する場合は原則自己負担になる見込みである。
2021年7月12日、第一三共はmRNAワクチンの臨床試験を年内に開始すると発表した。国内では既に他のワクチン接種が始まっていることから偽薬との比較は倫理上の問題があるため、他のワクチンとの効果の差を比較する劣性試験を行う予定。
2021年12月16日、武田薬品工業はアメリカのバイオテクノロジー企業ノババックスの組み換えタンパクワクチンについて、厚生労働省へ製造販売承認申請を行ったと発表した。2022年4月19日、厚生労働省はノババックス製の組み換えタンパクワクチン「ヌバキソビッド」について正式に製造販売を承認した。なお、ノババックスの組み換えタンパクワクチンの法令上の名称は「組換えコロナウイルス(SARS-CoV-2)ワクチン」である。
2022年9月20日、オミクロン株のBA.1に対応した従来株との2価ワクチンの接種を開始した。12歳以上の3回目以降の接種希望者(ブースター接種)が対象となる。
日本政府は2021年6月に「ワクチン開発・生産体制強化戦略」を閣議決定しており、これに基づいて国立研究開発法人日本医療研究開発機構が2022年3月22日にワクチン開発を手掛ける先進的研究開発戦略センター(SCARDA)を設立した。
KMバイオロジクスでは2023年の実用化を目指し不活化ワクチンの開発を進めている。
中国
2020年1月26日、中国CDC(疾病管理予防センター)の関係者は、ワクチンの開発を開始したと語った。1月29日、広州のロシア領事館は新型コロナウイルスのゲノムが中国からロシアに提供され、中露がワクチンの共同開発に着手したと発表した。
(上記と同じものかどうかは不明であるが)開発したワクチンの治験開始が3月17日に中国で承認され、陳薇をリーダーとする中国人民解放軍軍事科学院軍事医学研究院の研究者らが治験を開始。3月18日に中国中央電視台も報道した。
3月23日、軍事科学院軍事医学研究院生物工程研究所とカンシノ・バイオロジクスは、独自に開発した新型コロナウイルスワクチン(アデノウイルス媒体)の108人への第1期臨床試験を開始すると報道した。プロジェクト責任者は陳薇 (Chen Wei) 少将で、複製欠陥型ヒト5型アデノウイルスを媒体とし、新型ウイルスのS抗原を作る。感染予防のため、陳薇チーム7人は既に接種済みである。陳薇少将はウイルスのワクチンの研究で博士号を取得しており、これまでに抗SARSウイルス製剤やエボラ出血熱のワクチン開発に成功したと発表されている。
2020年5月25日、カンシノ・バイオロジクスは、同年3月から開始していたウイルスベクターワクチンの第1相臨床試験で、ヒトへの効果を世界で初めて確認したと報告した。6月25日、中華人民共和国中央軍事委員会は国産ワクチン「Ad5-nCoV」の使用を中国人民解放軍に限定して認可したことを決定した。7月22日より、医療従事者らを対象にワクチンの緊急使用を開始した。
2020年12月30日、中国のシノファーム社は国産ワクチン「BBIBP-CorV」の有効性を79.34%とし、同年12月9日に中国より先にワクチンを承認して首相のムハンマド・ビン・ラーシド・アール・マクトゥームらが接種していたアラブ首長国連邦が発表した86%よりも低く発表した。翌31日、中国の国家薬品監督管理局はシノファームの「BBIBP-CorV」を承認した。
2021年2月、中国の国家薬品監督管理局はシノバック・バイオテック社のCoronaVacとカンシノ・バイオロジクス社の国産ワクチン2種類を承認した。
2021年5月、世界保健機関は欧米以外のワクチンでは初めてシノファーム社のBBIBP-CorVの緊急使用を承認し、有効性は79%と推定した。
ロシア
2020年8月中旬にロシア政府が国内で製造されたワクチンを薬事承認し、10月以降医療従事者などを対象とした接種を開始する予定と発表した。その後、8月11日にウラジーミル・プーチン大統領がガマレヤ記念国立疫学・微生物学研究センターの国産ワクチン「Gam-COVID-Vac」(スプートニクV)を世界に先駆けて認可したことを発表した。
2020年11月11日、スプートニクVが発症を防ぐ有効性が92%に上ったとする最終第3段階の臨床試験の第1回中間結果をロシアは発表した。
アメリカ合衆国
アメリカ合衆国連邦政府は2020年、ワクチンの研究・製造への補助や買取事前契約などに100億ドル以上を投じる「オペレーション・ワープ・スピード」(超高速作戦)を開始した。アメリカ生物医学先端研究開発局はアストラゼネカ(イギリス)やサノフィ(フランス)など他国の製薬企業のワクチン開発も支援している。
2020年1月21日、アメリカの感染症薬メーカー、ノババックス(Novavax Inc.) は、本ウイルスの感染予防のためのワクチンの開発を始めたと語った。
2020年1月29日、米医薬品・日用品大手ジョンソン・エンド・ジョンソン (J&J) は、COVID-19 ワクチンの開発に着手したと発表した。エボラ出血熱のワクチン開発に利用した技術を応用する。このワクチンは現在、コンゴ民主共和国とルワンダで投与されている。「すでに多数の研究者をワクチン開発に投入しており、1カ月以内には何らかの成果が出せると確信している。世界市場に向けた量産体制はすでに整っているので、ワクチンが完成すれば、1年以内に億単位の出荷が可能」という。
2020年3月16日、アメリカ国立衛生研究所は、アメリカ国立アレルギー・感染症研究所とバイオ医薬企業のモデルナが開発していたmRNAワクチンが治験に至ったことを発表。治験は、ワシントン州シアトル市内で始まり、同年5月18日までに複数の治験参加者から抗体を確認することができた。全世界に1年間で5〜10億回分の供給を計画している。
ファイザーのワクチンが2020年に供給開始予定。2021年までに数億人規模の接種を目指す。日本にはワクチンが完成した場合には、2021年6月までに1億2,000回分を供給することで、日本国政府と基本合意されている。その後、2020年11月9日に初期の治験のデータが発表され、予防の有効性が90%越えとなった。これを受け、2020年11月中にもアメリカの食品医薬品局に承認の申請を行う。
ノババックスのワクチンは、1年に1億回分の生産を目標としている。生産はアメリカ合衆国の富士フイルム子会社と協力し、日本では武田薬品工業が原薬から製造し販売する予定。
イギリス
アストラゼネカがオックスフォード大学と共同でワクチン開発を開始し、そ2020年4月より臨床試験を開始した。同年9月以降、翌21年にかけて10億回分の生産が可能と目され、5月の時点で既に4億回分(アメリカ3億回分、イギリス1億回分)の供給を9月から開始することが予定されていた。その後に供給計画を20億回分に増加し、日本には1億2,000万回分、うち3,000万回分は2021年3月までに供給することをが日本国政府と基本合意された。治験については、参加者の中に深刻な副反応の疑いが確認されたため、9月9日から中断していた が、9月12日に再開したことを明らかにした。
しかし、アストラゼネカのワクチンについてはその後、各国で懸念が示されることとなる。2021年1月29日にはフランスのエマニュエル・マクロン大統領が、同社製のワクチンは60 - 65歳以上の高齢者にはほぼ効果がないと発言し、同国保健当局が2月2日に65歳以上の高齢者には接種しないよう勧告したのをはじめ、ドイツ、イタリア、スウェーデンの保健当局も高齢者への接種を行わないよう勧告した。ただし、欧州医薬品庁(EMA)は全年齢層の成人への接種を推奨した。
また2021年3月になってアストラゼネカ製のワクチンに接種後に血栓が発生するなどの副反応事例が報告されたためドイツ、フランス、イタリア、スペイン、デンマーク、アイスランド、ノルウェー、オランダ、タイ など接種を中断する国が続出した。3月15日にはWHOが同社製ワクチンと血栓の発生に因果関係は認められず、ワクチン接種を継続するようコメントを発表する事態となった。これを受けフランスやドイツでは接種を再開した。
アストラゼネカによる臨床試験では79%の有効性が確認されたと2021年3月22日に発表されている。しかしアメリカ国立アレルギー・感染症研究所は、古い不完全な治験データが含まれていた可能性があると指摘し、最新の正確な情報を提供するよう要求。アストラゼネカも48時間以内の最新データ提供を表明した。その結果、有効性は76%へと訂正された。
フランス
2020年2月18日、フランスのサノフィは、米国保健福祉省 (HHS) の生物医学先端研究開発局 (BARDA) と協力して、COVID-19のための遺伝子組換えワクチンの速やかな開発を目指すと発表した。アメリカ生物医学先端研究開発局からも支援を受けている。
インド
インドでは国産ワクチン2種の接種が2021年1月16日に開始された。インドには世界最大級のワクチン製造機関であるインド血清研究所(SII)があり、輸出も行われているが、原材料はアメリカやEUからの輸入に頼っている。
国内で流通するのは国内の製薬企業バーラト・バイオテック社とインド医学研究評議会が共同開発しSIIで製造されている「コバクシン」 と、アストラゼネカが開発しバーラト・バイオテックがライセンス生産する「コビシールド」であり、前者は承認段階で有効性を証明するデータが示されていなかった。その後の治験では有効性81%と評価されている。
台湾
台湾では、メディジェン・ワクチン・バイオロジクス(中国語: 高端疫苗生物製剤、新竹県)がアメリカ国立衛生研究所の協力を得て開発したMVC COVID-19ワクチン対して2021年7月に緊急使用許可が出された。2021年8月23日に接種が開始され、蔡英文総統は同日早朝に率先して接種を受けた。
蔡英文は、従来は中国の妨害により民間の調達や日本やアメリカからの無償供与以外ではワクチンの輸入が難しかったと述べている。
東南アジア諸国
ベトナムのナノジェン製薬バイオテクノロジーはベトナム軍医大学と共同で「ナノコバックス」を開発中であり、2021年2月に第2段階の治験、6月10日に最終段階の治験を開始した。
インドネシアではアイルランガ大学など7つの研究機関が開発中。
タイ王国ではタイ製薬公団(GPO)とマヒドン大学熱帯医学部が共同開発を進めている。
イラン
イランの最高指導者アリー・ハーメネイーが2021年6月25日に接種を受けたワクチンは、イランで開発されている複数のワクチンのうち、同月に緊急承認されたものとイラン国営メディアにより報道された。
キューバ
キューバは、WHO未承認であるものの国産ワクチンを製造しており、2021年9月16日には子供(2 - 11歳)にも接種対象を広げた。
韓国
2022年6月29日、韓国政府はSKバイオサイエンス社が開発した新型コロナウイルスのワクチンを認可したと発表した。韓国の国産ワクチンの認可は初めて。新型コロナのワクチンと治療薬両方を独自に開発・生産するのは米英に続き3カ国目。当局によると、同ワクチンは冷蔵保管が可能で、超低温冷凍などは不要。一方、オミクロン変異株などに対する有効性は「研究中」としており、具体的な供給計画は固まっていない。
ワクチンの種類
2021年1月時点、COVID-19に対する有効なワクチンを作成するために、9つの異なる技術プラットフォーム(多数の候補の技術が未定義のまま)が研究開発中である。
臨床試験中のワクチン候補のプラットフォームのほとんどは、COVID-19感染の主要抗原としてのコロナウイルススパイクタンパク質とその変異体に焦点を当てている。2020年に開発されたプラットフォームには、核酸技術(ヌクレオシド修飾メッセンジャーRNAおよびDNA)、非複製ウイルスベクター、ペプチド、組換えタンパク質、弱毒化ウイルス、不活化ウイルスなどがある。
COVID-19のために開発されている多くのワクチン技術は、インフルエンザを予防するために既に使用されているワクチンとは異なり、COVID‑19感染メカニズムの精度を高めるために「次世代」戦略を使用している。いくつかの合成ワクチンでは、2P変異を利用してスパイクタンパク質を融合前構造に固定し、ウイルスがヒトの細胞に付着する前に免疫応答を刺激する。開発中のワクチンプラットフォームは、抗原操作の柔軟性を高め、医療従事者、高齢者、子供、妊婦、免疫力が低下している人など、COVID-19の感染しやすい人々の感染メカニズムをターゲットとした効果が期待できる。。
SARS-CoV-2タンパク質を形成して免疫反応を促すための3種類のワクチンを示す概念図。(1)RNAワクチン、(2)サブユニットワクチン、(3)ウイルスベクターワクチン
SARS-CoV-2に採用されているワクチンのプラットフォーム。全ウイルスワクチンには、弱毒化されたウイルスと不活性化されたウイルスの両方が含まれる。タンパク質およびペプチドサブユニットワクチンは通常、免疫原性を高めるためにアジュバントと組み合わされる。SARS-CoV-2ワクチン開発では、三量体のスパイクタンパク質全体、または受容体結合領域(RBD)などの構成要素を使用することに重点が置かれている。複数の非複製ウイルスベクターワクチンが開発されており、特にアデノウイルスに焦点が当てられている。一方、複製ウイルスベクターのコンストラクトはあまり重視されていない。
RNAワクチン
RNAワクチンにはRNAが含まれており、組織に導入されるとメッセンジャーRNA(mRNA)として働き、細胞に外来タンパク質を作らせ、適応免疫反応を刺激して、対応する病原体やがん細胞を識別して破壊する方法を体に教える。RNAワクチンは、ヌクレオシド修飾メッセンジャーRNAを使用することがよくあるが、必ずしもそうとは限らない。mRNAの送達は、RNA鎖を保護し、細胞への吸収を助ける脂質ナノ粒子に分子を共製剤化することによって実現される。この技術の開発は、ペンシルベニア大学の免疫学者、ドリュー・ワイスマンとカリコー・カタリンによる。
RNAワクチンは、米国および欧州連合で認可された最初のCOVID-19ワクチンである。2021年1月時点、このタイプの認可されたワクチンは、ファイザー-バイオンテックワクチン とモデルナワクチン である。2021年2月現在、EUではCureVac社のCVnCoV RNAワクチンが認可を待っている。
重度のアレルギー反応はまれである。2020年12月、ファイザー-バイオンテックCOVID-19ワクチンの初回投与1,893,360回では、重度のアレルギー反応が175例発生し、そのうち21件がアナフィラキシーであった。2020年12月および2021年1月に行われたモデルナ COVID-19ワクチンの4,041,396回の投与では、アナフィラキシーの報告は10件のみであった。脂質ナノ粒子がアレルギー反応に関与している可能性が最も高い。
アデノウイルス・ベクター・ワクチン
これらのワクチンは、SARS-CoV-2タンパク質をコードするDNAを含むアデノウイルス・シェルを用いた、非複製ウイルスベクターの例である。COVID-19に対するウイルスベクターを用いたワクチンは、新しいウイルス粒子を生成するのではなく、全身の免疫反応を誘発する抗原のみを生成するという非複製性を持っている。
2021年1月時点、このタイプのワクチンとして認可されているのは、英国のオックスフォード-アストラゼネカワクチン、ロシアのスプートニクV、中国のコンビディシア、そしてジョンソン・エンド・ジョンソンワクチンである。
コンビディシアとジョンソン・エンド・ジョンソンのワクチンは、いずれもワンショットワクチンで、物流の煩雑さがなく、通常の冷蔵保存で数か月間保存できる。
スプートニクVは、ジョンソン・エンド・ジョンソン社のワクチンと同じAd26を1回目に使用し、コンビディシアと同じAd5を2回目に使用しており、単回投与と同様の有効性を得ることができ、1回の投与で同じ効果があるか完全試験が行われている。
不活化ウイルスワクチン
不活化ワクチンとは、培養したウイルス粒子を熱やホルムアルデヒドなどの方法で死滅させることにより、病気を引き起こす能力を失わせ、かつ免疫反応を起こさせるワクチンである。
2021年1月時点、中国のCoronaVac、BBIBP-CorV、IBP-CorV、インドのCovaxin、ロシアのCoviVac が認可されている。臨床試験中のワクチンには、KMバイオロジクスやValneva社のワクチンがある。
サブユニットワクチン
サブユニットワクチンは、病原体の粒子全体を導入することなく、1つまたは複数の抗原を提示する。抗原はしばしばタンパク質サブユニットであるが、病原体の断片であればどのような分子でもよいとされている。
2021年4月時点、このタイプのワクチンとして承認されているのは、ペプチドワクチンのEpiVacCorona とRBD-Dimer の2つである。認可が保留されているワクチンには、Novavax COVID-19ワクチン と、SOVERANA 02(コンジュゲートワクチン)、Sanofi-GSKワクチンがある。V451ワクチンは以前、臨床試験が行われていたが、その後のHIV検査で誤った結果を引き起こす可能性があることが判明したため中止された。
自己増殖型RNAワクチン
自己増殖RNAワクチンや自己複製RNAワクチンと呼ばれる、自ら増殖や複製するワクチンである。次世代のRNAワクチンであり、接種後に体内でRNAを増やすタンパク質を増殖させ、自らRNAを増やすワクチンである。VLPセラピューティクス・ジャパンしたワクチンの場合、自ら増殖するため、レプリコンの粒子が127gあれば、日本の全人口に接種出来るだけのワクチンが作れる計算になるとされる。また、保管も4°Cの環境で1 - 2か月は保存可能であるとされる。VLPセラピューティクス・ジャパン、大阪市立大学、国立国際医療研究センター、医薬基盤・健康・栄養研究所、大分大学などが開発中である。他にも米国メリーランド州ボルチモアのElixirgen Therapeutics, Inc.(エリクサジェン・セラピューティックス社)が自己複製型RNAワクチン「EXG-5003」を開発し、日本では藤田医科大学(愛知県豊明市)にて、第 1/2 相臨床試験を開始している。
その他の種類
臨床試験が行われているその他のワクチンには、ウイルス様粒子ワクチン、複数のDNAプラスミドワクチン
経口ワクチンや経鼻ワクチンも開発・研究されている。経鼻ワクチンについては、タデ藍(青森県産の『あおもり藍』)の葉から抽出したエキス(トリプタンスリン含有)が、ウイルスの細胞への侵入を防ぐ働きを持つことや、自然素材で副作用が少ないことから、藍の葉のエキスを配合した点鼻薬の市販化を目指している。
終生免疫の獲得を目指したワクチンの研究開発もおこなわれており、東京都医学総合研究所が研究開発する天然痘ワクチンであるワクシニアウイルスを更に弱毒化したDIs株に、SARS-CoV-2遺伝子を組み込んだ遺伝子組換え生ワクチンや、東京大学生産技術研究所が麻疹ウイルスをベクターとして用いた遺伝子組換え生ワクチンを研究開発している 。
科学者たちは、関連性のない疾患に対する既存のワクチンが、免疫系を活性化し、COVID-19感染の重症度を軽減できるかどうかを調査した。結核用のBCGワクチンが免疫系に非特異的な作用を及ぼすという実験的証拠はあるが、このワクチンがCOVID-19に有効であるという証拠はない。
有効性
ワクチン有効性(vaccine efficacy)とは対照試験において、ワクチンを接種した被験者が病気にかかるリスクと、ワクチンを接種していない被験者が病気にかかるリスクを比較したものである。有効性0%とは、ワクチンが効かないことを意味する(プラセボと同じ)。 有効性が50%の場合は、ワクチン未接種の人と比べてワクチン接種した人の感染症例が半分になることを意味する。
臨床試験は、異なる集団、地域、ウイルスの亜種を用いて実施されたため、異なるワクチンの有効性を比較するのは簡単ではない。COVID-19の場合、ワクチン有効率が67%であればパンデミックを遅らせるのに十分かもしれないが、これはワクチンが感染を防ぐために必要な殺菌免疫(ウイルスを感染前に排除する免疫系の作用)を与えることを前提としている。ワクチン有効性は疾病予防を反映したものであり、無症状の人は感染力が強い可能性があるため、SARS-CoV-2の感染性を示す指標としては不十分である。米国食品医薬品局(FDA)と欧州医薬品庁(EMA)は、COVID-19ワクチンの承認に必要な有効性として50%をカットオフ値として設定している。現実的な集団ワクチン接種率を75%を目標とし、実際の基本再生産数に応じてCOVID-19ワクチンに必要な有効性は、流行を防ぐためには70%以上、社会的距離を置くなどの措置をとらずに流行を消滅させるためには80%以上であると予想されている。
有効性の計算において、症候性COVID-19とは、一般的にPCR(ポリメラーゼ連鎖反応)検査が陽性であり、かつCOVID-19の症状の定義済リストのうち少なくとも1つまたは2つの症状を有するものと定義されているが、正確な仕様は試験によって異なる。国によってSARS-CoV-2変異株の有病率が異なるため、試験場所も報告された有効性に影響を与える。以下の範囲は、特に記載のない限り95%信頼区間であり、全ての値は年齢に関係なく全ての被験者に対するものである。重症化したCOVID-19に対する有効性は最も重要で、入院や死亡が公衆衛生上の負担となり、その予防が優先される。認可・承認されているワクチンでは、以下のような有効性が示されている。
| ワクチン | COVID-19の重症度による有効性 | 臨床試験実施場所 | 参照先 | ||
|---|---|---|---|---|---|
| 軽度または中等度 | 入院や死亡を伴わない重篤な症状 | 入院や死亡を伴う重篤な症状 | |||
| モデルナワクチン | ~94% (89–97%) | ~100% | ~100% | United States | |
| ファイザーバイオンテックワクチン | ~95% (90–98%) | Not reported | Not reported | Multinational | |
| スプートニク・ライト | ~79% | Not reported | Not reported | Russia | |
| スプートニクVワクチン | ~92% (86–95%) | ~100% (94–100%) | ~100% | Russia | |
| オックスフォード-アストラゼネカワクチン | ~81% (60–91%) | ~100% (72–100%) | ~100% | Multinational | |
| ~76% (68–82%) | ~100% | ~100% | United States | ||
| BBIBP-CorV | ~79% | ~100% | ~100% | Multinational | |
| CoronaVac | ~78% | ~100% | ~100% | Brazil | |
| ノババックスワクチン | ~89% (75–95%) | ~100% | ~100% | United Kingdom | |
| ~60% (20–80%) | ~100% | ~100% | South Africa | ||
| ジョンソン・エンド・ジョンソンワクチン | ~66% (55–75%) | ~85% (54–97%) | ~100% | Multinational | |
| ~72% (58–82%) | ~86% (−9–100%) | ~100% | United States | ||
| ~68% (49–81%) | ~88% (8–100%) | ~100% | Brazil | ||
| ~64% (41–79%) | ~82% (46–95%) | ~100% | South Africa | ||
| Covaxin | ~78% (61-88%) | ~100% | ~100% | India | |
| Convidicea | ~66% | ~91% | Not reported | Multinational | |
ワクチン実効性
ワクチン実効性(vaccine effectiveness)に関する実社会での研究では、特定のワクチンが、理想的とは言えない日常的な条件下で、大規模な集団におけるワクチン接種者のCOVID-19の感染、症状、入院、死亡をどの程度防ぐことができたかを測定する。
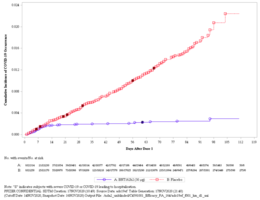
- イスラエルでは、2020年12月20日から2021年1月28日までの期間にモデルナまたはファイザー-バイオンテックのワクチンを接種した715,425人のうち、2回目の接種から7日後からの期間に、317人(0.04%)のみが軽度/中等度のCovid-19症状で発病し、16人(0.002%)のみが入院したことが確認された。
- 米国疾病予防管理センターの報告書によると、ファイザー-バイオンテック社およびモデルナ社のCovid-19ワクチンは、非常に効果的な防御を提供する。実際の環境下では、症状の状態にかかわらず、SARS-CoV-2感染に対して、完全免疫(2回目の投与から14日以上後)のmRNAワクチンの実効性は90%、部分免疫(1回目の投与から14日以上で2回目の投与前)のワクチン実効性は80%であった。
- 英国の104の病院に勤務する15,121人の医療従事者は、調査前に全員のCOVID-19抗体が陰性であったが、2020年12月7日から2021年2月5日まで、系統 B.1.1.7が優勢変異株として循環していた時期に、週2回の逆転写ポリメラーゼ連鎖反応(RT-PCR)検査で追跡調査を行った。この研究では、ワクチンを接種した90.7%のコホート(母集団)と、ワクチンを接種しなかった9.3%のコホートの陽性結果を比較し、ファイザー-バイオンテック社のワクチンは、全ての感染症(無症候性を含む)を、1回目の接種から3週間後には72%(58-86%)減少させ、2回目の接種から1週間後には86%(76-97%)減少させたことがわかった。
- 2021年1月17日から3月6日まで、系統B.1.1.7が優勢変異株として循環していた時期に、イスラエルの一般住民を対象に行われた研究では、ファイザー社ワクチンにより、無症候性COVID-19感染症が94%、症候性COVID-19感染症が97%減少したことが明らかになった。
- アメリカのメイヨー・クリニックの術前患者を対象とした研究では、mRNAワクチンが無症候性感染症に対して80%の防御効果があることが示された。
- 中国疾病管理センターの所長である高福は、2021年4月10日に開催された会議で、中国製ワクチンは「防御率はあまり高くない」と認めた。民間企業であるシノバック社が開発したCoronaVacワクチンは、ブラジルでの臨床試験で有効率が50.4%にとどまることが判明した。トルコで行われた別の試験では、83.5%の実効性が示された。国営のシノファーム社によると、その2つのワクチンの有効率は79.4%と72.5%である。
| ワクチン | COVID-19の重症度別の実効性 | 調査国 | Refs | ||
|---|---|---|---|---|---|
| 無症候 | 症候性 | 死亡 | |||
| ファイザー-バイオンテック | 〜86% (76-97%) | Not reported | United Kingdom | ||
| 〜90% (68-97%) | 〜100% | United States | |||
| 〜94% | 〜97% | Israel | |||
| モデルナ | 〜90% (68-97%) | 〜100% | United States | ||
| CoronaVac | Not reported | 〜67% (65-69%) | 〜80% (73-86%) | Chile | |
| スプートニクV | Not reported | 〜98% | Not reported | Russia | |
変異株に対する有効性
現行のCOVID-19ワクチンによって誘発される抗体応答に対して中程度または完全に耐性を持つSARS-CoV-2変異株が出現した場合、ワクチンの変更が必要になる可能性がある。初期株用に開発された多くのワクチンが、症候性COVID-19の一部の変異株に対する有効性が低いことが試験で示されている。2021年2月の時点で、米国食品医薬品局(FDA)は、FDAが認可した全てのワクチンはSARS-CoV-2の循環株に対する保護効果を維持していると捉えている。
変異株は、回復者やワクチン接種者が獲得する中和抗体から逃避するリスクが懸念されているが、国立感染症研究所と日本医療研究開発機構の研究にて、新型コロナウイルス感染症(COVID-19)回復者の中和抗体の総量は時間と共に減衰するが、変異株に交差結合する抗体を獲得し、この抗体の質(中和比活性・交差性)は時間と共に向上することを発見した。この現象は、変異株へのワクチン戦略に重要な知見になるとしている 。
アルファ株(系統 B.1.1.7)
2020年12月、英国で新たな変異株である系統 B.1.1.7が確認された。初期の結果では、ファイザー-バイオンテックワクチンとモデルナワクチンの両方が英国の変異株に対して保護することを示唆している。
ある研究では、オックスフォード-アストラゼネカワクチンは、B.1.1.7に対して42〜89%の有効性を示し、B.1.1.7以外の変異株に対しては71〜91%の有効性を示した。臨床試験の予備データによると、Novavaxワクチンは、オリジナルの変異株に対して〜96%、B.1.1.7に対して〜86%、南アフリカのB.1.351(501.V2 変異株)に対して〜60%の症状改善効果があることが示されている。
ベータ株(系統 B.1.351/501.V2 変異株)
モデルナは、南アフリカの系統 B.1.351(501.V2 変異株)に取り組むための新しいワクチンの試験を開始した。2021年2月17日、ファイザーはB.1.351の中和活性が2/3に低下したと発表したが、この変異株に対するワクチンの疾病予防効果については、まだ主張できないとしている。B.1.351に対するモデルナおよびファイザーのワクチンを接種した患者からの血清の中和活性の低下は、その後、いくつかの研究で確認された。4月1日、ファイザー-バイオンテックによる南アフリカでのワクチン試験の最新情報では、ワクチンの効果は今のところ100%(つまり、ワクチンを接種した被験者には症例が発生しなかった)で、プラセボ対照群では9件の感染のうち6件がB.1.351であったと述べられている。
2021年1月、南アフリカでAd26.COV2.S ワクチンの臨床試験を実施したジョンソン・エンド・ジョンソンは、中等度から重度のCOVID-19感染に対する防御レベルは、米国で72%、南アフリカで57%であったと報告した。
2月6日、『フィナンシャル・タイムズ』紙は、南アフリカのウィットウォーターズランド大学がオックスフォード大学と共同で実施した試験の暫定試験データで、オックスフォード-アストラゼネカワクチン(AZD1222)のB.1.351に対する有効性の低下を示したと報じた。この研究では、2,000人のサンプルサイズにおいて、AZD1222 ワクチンは、COVID-19の最も重篤な症例を除く全ての症例において「最小限の保護」しか提供しないことが分かった。2月7日、南アフリカ保健大臣はデータを検討し、どのように進めるべきかアドバイスを待つ間、約100万回分のワクチンの配備計画を中止した。
ガンマ株(系統 P.1)
ブラジルで最初に同定された変異株である系統 P.1(20J/501Y.V3)は、ファイザー-バイオンテックによるワクチン接種の効果を部分的に免れている可能性がある。
系統 B.1.617(デルタ株/カッパ株)
2020年10月、インドで新たな二重変異変異体が発見され、系統 B.1.617と名付けられた。2021年1月まではほとんど検出されず、4月には南極大陸と南米大陸を除く各大陸の少なくとも20カ国に広がった。約15種ある定義された変異の中で、これにはスパイク変異D111D(同義)、G142D、P681R、E484Q、L452R があり、後者の2つは容易に抗体を回避する原因になる可能性がある(※後述の系統 B.1.617.2にはG142DとE484Qの変異がなく、代わりにT478K変異がある)。
なお、亜系統として系統 B.1.617.1(カッパ株)、系統 B.1.617.2(デルタ株)、系統 B.1.617.3の3つがあり、系統 B.1.617.2はWHOなどにより懸念される変異株 (VOC) に指定されている。
デルタ株はウイルス量が多く、感染力が強いとされている。ワクチンを打っていたとしても従来株に比べ感染するリスクが高くなっている、一方でワクチンの効果により重症化リスクは低く抑えられている。また、ワクチン接種者が感染した場合でも、軽症や無症状であったとしても、ワクチン非接種者と同様に体内で大量に増殖しウイルスの感染源となる可能性が指摘されている。
臨床試験および認可状況
第I相試験では、主に数十人の健康な被験者を対象に安全性と予備的投与量を試験し、第II相試験では、第I相試験の成功を受けて免疫原性、投与量レベル(バイオマーカーに基づく有効性)、および候補ワクチンの副作用を評価し、通常は数百人を対象としている。第I–II相試験は、予備的な安全性と免疫原性試験で構成され、通常は無作為化、プラセボ対照試験で、より正確で効果的な用量を決定する。第III相試験では通常、複数の施設でより多くの被験者が参加し、対照群を含めて、最適な用量で有害作用を監視しながら、病気を予防するためのワクチンの有効性を試験する(「介入試験」または「ピボタル試験」)。第III相試験におけるワクチンの安全性、有効性、および臨床エンドポイントの定義は、副作用の程度、感染または感染量の定義、ワクチンが中等度または重度のCOVID-19感染を予防するかどうかなど、各社の試験によって異なる場合がある。
進行中の臨床試験の計画は、試験でデータを蓄積することにより、治療法の有効性についての肯定的または否定的な早期の洞察が得られる場合には、適応デザインとして変更されることがある。候補ワクチンに関する進行中の第II-III相臨床試験における適応デザインは、試験期間を短縮し、被験者数を減らすことができ、早期終了または成功の判断を迅速化し、研究努力の重複を回避し、国際的な拠点間での連帯試験(Solidarity trial)の計画変更について調整を強化する。
認可または承認されたワクチンのリスト
各国の規制当局は、22種のワクチンの緊急使用許可を与えている。そのうち6つのワクチンは、少なくとも1つのWHO認定の厳格な規制当局によって緊急使用または一般使用が承認されている。
| ワクチン候補薬、開発者、出資者 | 開発国 | ワクチン種類(技術) | 接種間隔 | 保管温度 | 現在の相(被験者数) | 承認数 | 緊急使用許可数 |
|---|---|---|---|---|---|---|---|
|
オックスフォードアストラゼネカCOVID-19ワクチン (Vaxzevria, コビシールド) オックスフォード大学、アストラゼネカ、CEPI |
英国 | アデノウイルス ベクター (ChAdOx1) | 2回
4-12週 |
2-8℃ | 第III相 (30,000) | 2 | 143 |
|
ファイザー-バイオンテックCOVID-19ワクチン (コミナティ, トジナメラン) バイオンテック、ファイザー |
米国、ドイツ | RNA (modRNAを脂質ナノ粒子に分散) | 2回
3-4週 |
-70±10℃ |
第III相 (43,448) | 5 | 93 |
| スプートニクV COVID-19ワクチン (Gam-COVID-Vac) | ロシア | アデノウイルス ベクター (組み換えワクチン、Ad5およびAd26型) | 2回
3週 |
-18 ℃ (冷凍庫) | 第III相 (40,000) | 2 | 6 |
|
モデルナCOVID-19ワクチン モデルナ、NIAID、BARDA、CEPI |
米国 | RNA (modRNAを脂質ナノ粒子に分散) | 2回
4週 |
-20±5℃ (冷凍庫) | 第III相 (30,000) | 2 | 50 |
|
BBIBP-CorV シノファーム: 北京生物製品研究所 |
中国 | 不活化 SARS-CoV-2 (ベロ細胞) | 2回
3-4週 |
2-8℃ | 第III相 (48,000) | 4 | 50 |
|
ジョンソン・エンド・ジョンソンCOVID-19ワクチン ヤンセン ファーマ、ジョンソン・エンド・ジョンソン、BIDMC |
米国、オランダ | アデノウイルス ベクター (組み換えワクチン、Ad26) | 1回 | 2-8℃ | 第III相 (40,000) | 0 | 46 |
|
CoronaVac シノバック |
中国 | 不活化 SARS-CoV-2 (ベロ細胞) | 2回
2週 |
2-8℃ | 第III相 (33,620) | 1 | 32 |
|
BBV152 (コバクシン) Bharat Biotech、インド医学研究評議会 |
インド | 不活化 SARS-CoV-2 (ベロ細胞) | 2回
4週 |
2-8℃ | 第III相 (25,800) | 0 | 14 |
|
Ad5-nCoV (コンビディシア) CanSinoBIO, 中国陸軍医科学院 |
中国 | アデノウイルス ベクター (組み換えワクチン、Ad5) | 1回 | 2-8℃ | 第III相 (40,000) | 1 | 5 |
|
EpiVacCorona Vector Institute |
ロシア | サブユニット (ペプチド) | 2回
3週 |
2-8℃ | 第III相 (40,000) | 1 | 2 |
|
ZF2001(RBD-Dimer) Anhui Zhifei Longcom Biopharmaceutical Co. Ltd. |
中国 | サブユニットワクチン(組み換えワクチン) | 3回
30日 |
第III相 (29,000) | 0 | 2 | |
|
WIBP-CorV
シノファーム: 武漢生物製品研究所 |
中国 | 不活化 SARS-CoV-2 (ベロ細胞) | 1回 | 第III相 (51,600) | 0 | 2 | |
|
CoviVac The Chumakov Centre at the Russian Academy of Sciences |
ロシア | 不活化 SARS-CoV-2 | 2回
2週 |
2-8℃ | 第III相 (3,000) | 0 | 1 |
|
QazCovid-in (QazVac) Research Institute for Biological Safety Problems |
カザフスタン | 不活化 SARS-CoV-2 | 2回
3週 |
2-8℃ | 第III相 (3,000) | 0 | 1 |
| スプートニク・ライト | ロシア | アデノウイルス ベクター (組み換えワクチン、Ad26型) | 1回 | 2-8℃ | 第III相 (7,000) | 0 | 3 |
|
'''高端(メディジェン)COVID-19ワクチン'''(英語: MVC-COV1901) Medigen Vaccine Biologics(中国語: 高端疫苗生物製劑), Dynavax Technologies |
台湾 | サブユニットワクチン(S-2Pタンパク質+CpG 1018) | 2回
28日 |
2-8℃ | 第III相 (5,120) | 0 | 3 |
ヒト臨床試験中のワクチン候補
製剤
2020年現在、臨床開発中のワクチン候補のうち11種は、免疫原性を高めるためにアジュバントを使用している。免疫アジュバントとは、COVID-19ウイルスやインフルエンザウイルスなどの抗原に対する免疫反応を高めるためにワクチンに配合される物質である。具体的には、アジュバントを使用してCOVID-19ワクチン候補を製剤化し、その免疫原性と有効性を高めて、ワクチン接種を受けた個体におけるCOVID-19感染を低減または予防することができる。COVID-19ワクチンの製剤化で使用されるアジュバントは、不活化COVID-19ウイルス、および組換えタンパク質ベース、またはベクターベースのワクチンを使用する技術において特に効果的となる可能性がある。ミョウバンとして知られるアルミニウム塩は、認可されたワクチンに使用された最初のアジュバントであり、アジュバント化ワクチンの約80%で選択されるアジュバントである。ミョウバンアジュバントは、炎症性サイトカインの放出を含む免疫原性を高めるために、多様な分子および細胞メカニズムを開始する。
費用
ある専門家によると、COVID-19に対する効果的なワクチンは、世界的な経済的影響において何兆ドルもの節約となる可能性があり、したがって、数十億ドルの費用はそれに比べれば小さく見えるという。 パンデミックの初期段階では、このウイルスに対する安全性・信頼性が高く、手頃な価格のワクチンを作成できるかどうかは知られておらず、ワクチン開発にどれくらいの費用がかかるかも正確には知られていなかった。 成功せずに何十億ドルもの投資が行われる可能性もあった。
効果的なワクチンが開発されると、数十億回分のワクチンを製造し、世界中に流通させる必要がある。2020年4月、ゲイツ財団は、製造と流通には250億米ドルもの費用がかかると見積もっている。第I相臨床試験では、ワクチン候補の84 - 90% が開発途中で最終承認に至らず、第III相臨床試験では25.7%が承認に至らない。ワクチン候補に対する製造業者の投資額は10億米ドルを超え、先進的な製造契約を結んだ場合には何百万もの投与が無駄に終わる可能性がある。
2020年11月現在、米国の「ワープ・スピード作戦(Operation Warp Speed)」プログラムの下で補助金を受けている企業は、初期価格をインフルエンザワクチンに合わせて1回あたり19.50米ドルから25米ドルに設定している。 2020年12月には、ベルギーの政治家がワクチン生産者とEUの間で合意された機密価格を簡単に公表した:
| 製造者 | ワクチン | EUにおける投与1回あたりの価格 |
|---|---|---|
| アストラゼネカ | オックスフォード-アストラゼネカCOVID-19ワクチン | €1.78 |
| ジョンソン・エンド・ジョンソン | ジョンソン・エンド・ジョンソンCOVID-19ワクチン | US$ 8.50 |
| サノフィ / GSK | €7.56 | |
| ファイザー / バイオンテック | ファイザー-バイオンテックCOVID-19ワクチン | €12.00 |
| CureVac | CureVac COVID-19ワクチン | €10.00 |
| R-Pharm | スプートニクV COVID-19ワクチン | US$ 10.00 |
| モデルナ | モデルナCOVID-19ワクチン | US$ 18.00 |
サプライチェーン
2021年以降にCOVID-19ワクチン接種を展開するには、100〜190億本(バイアル)の世界的な輸送と追跡が必要となる可能性があり、この取り組みは容易に史上最大のサプライチェーンの課題となる。2020年9月の時点で、サプライチェーンとロジスティクス(物流)の専門家は、認可ワクチンを流通させるための国際的および国内的なネットワークが量・緊急性ともに対応する準備ができていないと懸念を表明している。その理由は主に2020年のパンデミックのロックダウンと供給能力を低下させるダウンサイジングの間のリソースの悪化が原因としている。COVAX(The COVID-19 Vaccines Global Access)パートナーシップ、世界の製薬会社、契約ワクチンメーカー、国境を越えた輸送、保管施設、各国の保健機関など、多数の組織を調整することで直面している世界的な課題について、GAVIの最高経営責任者(CEO)であるセス・バークレーは次のように述べている。"何十億ものワクチンを効率的に全世界に届けるためには、サプライチェーンに沿った非常に複雑なロジスティックとプログラム上の障害を伴うことになる”。
課題の大きさを強調する例として、国際航空運送協会は、COVID-19パンデミックを経験している200カ国以上の人々に1回分の投与量のみを輸送するだけでも、8,000機の747型貨物機(精密ワクチン保冷装置を導入)が必要であると述べている。GAVIは、「動きの速いパンデミックでは、全員が安全でなければ誰も安全ではない」と述べている。
ワクチン技術や初期段階の臨床研究への数十億ドルの投資とは対照的に、ワクチンのライセンス取得後のサプライチェーンは、同様な計画、調整、セキュリティ、または投資を受けていない。主な懸念は、低・中所得国、特に子どもたちへのワクチン接種のためのワクチン流通資源が不足しているか、または存在しないということである。9月には、COVAXのパートナーシップには、172カ国がCOVID-19ワクチンのサプライチェーンを最適化するための計画を調整することが含まれており、国連児童基金(ユニセフ)はCOVAXと協力して、92の開発途上国における子どもたちのワクチン接種のための、資金調達とサプライチェーンを準備することになった。
物流
ワクチン接種のための物流サービスは、必要な機器、スタッフ、国際的な国境を越えた認可ワクチンの供給を保証するものである。物流の中核には、ワクチンの取り扱いとモニタリング、コールドチェーン管理、ワクチン接種ネットワーク内での流通の安全性などが含まれる。COVAX施設の目的は、製造、輸送、および全体的なサプライチェーンのインフラを統合し、参加国間の物流資源を一元化し、平等に管理することである。ワクチン予測とニーズ推定、国内ワクチン管理、無駄遣いの可能性、および在庫管理のための物流ツールが含まれている。
COVID-19ワクチンの輸送中に国際的に実施される他の物流要因には、以下のものがある:
- 個々のワクチンバイアルをバーコードによる可視化し、追跡可能にする(visibility and traceability)
- サプライヤー監査の共有化
- 製造から被接種者へのワクチンバイアル輸送証拠保全の共有化
- ワクチン温度監視ツールの使用
- 温度安定性試験と保証
- 新しい包装・配送技術
- 備蓄
- 各国内の物資調整(個人用保護具(PPE)、希釈剤、注射器、針、ゴム栓、冷凍庫の電源、廃棄物処理など
- 通信技術
- 各国の環境影響
あるワクチン開発者によると、いずれかの段階で物流が不足すると、サプライチェーン全体が脱線する可能性があるという。ワクチンのサプライチェーンが失敗した場合、パンデミックの経済的・人的コストは何年にもわたって長期化する可能性がある。
製造能力
2020年8月時点で、安全性と有効性の確立から数カ月が経過した段階で、いくつかのワクチン候補が第III相試験に入った段階にもかかわらず、多くの政府が50億米ドル以上の費用をかけて20億回分以上のワクチンを予約注文した。英国政府からの2021年のワクチン予約注文は、1人当たり5回分であった。9月には、CEPIは、2021年末までに認可された3種のワクチンを20億回分製造するという資金調達の約束の下、9種のワクチン候補の基礎研究と臨床研究を資金面で支援している。2022年までに全体で70億〜100億回分のCOVID-19ワクチンが世界中で製造される可能性があるが、富裕国による大量の事前注文(「ワクチンナショナリズム」と呼ばれる)は、より貧しい国のワクチン利用を脅かすものである。
インド血清研究所は、少なくとも10億回分のワクチンを生産する計画であるが、その半分はインドで使用されると述べている。
中国は、10月にCOVAXに参加した後、2020年末までに6億回分のワクチンを生産し、2021年にはさらに10億回分のワクチンを生産することを明らかにしたが、14億人の自国の人口に対して何回分のワクチンを生産するのかは不明であった。シノファーム社は、2021年に10億用量以上の生産能力を持つ可能性があると述べている。Sinovac社は、2020年末までに第2の生産施設を完成させ、CoronaVacの生産能力をそれまでの3億用量から6億用量に引き上げることを目指していると述べている。
アストラゼネカのパスカル・ソリオCEOは次のように述べている。"課題はワクチンそのものの製造ではなく、バイアルへの充填にある。世界には十分なバイアルが無い」 バイアル製造の高い需要に備えて、アメリカのガラスメーカーは7月にバイアル工場のために1億6,300万ドルを投資した。バイアル製造のためのガラスの入手可能性と、汚染物質の管理が懸念されているが、手頃な価格のワクチンが求められる中、製造コストの上昇と開発者の利益の可能性の低下を示している。
ワクチンは、国際的な規則を用いて取り扱われ、輸送され、ワクチン技術によって異なる温度管理された状態で維持され、保管中に劣化する前に予防接種に使用されなければならない。COVID-19ワクチンのサプライチェーンの規模は、脆弱な集団への世界的な配送を確実にするために、膨大なものになると予想される。このような流通のための施設を準備するための優先事項には、温度管理された施設や設備、インフラの最適化、予防接種スタッフの訓練、厳格なモニタリングが含まれる。RFID技術は、製造業者からワクチン接種までのサプライチェーン全体に沿ってワクチンの投与量を追跡し、認証するために実施されている。
2020年9月、グランドリバー・アセプティック・マニュファクチャリング社は、ジョンソン・エンド・ジョンソン社と、技術移転と充填・仕上げ製造を含むワクチン候補の製造を支援することで合意した。2020年10月には、2020年12月に最初の投与量を製造する予定のパートナーであるロンザグループが、スイスのフィスプでワクチン候補のモデルナを製造することが発表された。新たに建設された2,000平方メートルの施設では、年間3億投与量の製造が開始される予定である。ここで製造されたものは、製造の最終段階のために、スペインのLaboratorios Farmacéuticos Rovi SAに-70℃で冷凍出荷される予定である。ニューハンプシャー州ポーツマスにあるロンザの拠点は、早ければ11月にも米国専用のワクチン原料の製造を開始することを目指している。
コールドチェーン
ワクチン(およびアジュバント)は、温度変化に対して本質的に不安定であり、サプライチェーン全体を通してコールドチェーン管理を必要とし、通常は2〜8℃(36〜46°F)の温度で保たれる。COVID-19ワクチンの技術は、いくつかの新しい技術の中でも多様であるため、コールドチェーン管理には新たな課題があり、凍結中は安定しているが熱に弱いワクチンもあれば、凍結すべきではないワクチンもあり、また温度を超えて安定しているワクチンもある。凍結による損傷や、現地での接種プロセスにおける人員のトレーニング不足が大きな懸念事項である。複数のCOVID-19ワクチンが承認された場合、ワクチンのコールドチェーンは、気候条件や温度維持のための現地資源が変化する、異なる国の間で、これら全ての温度感受性に対応しなければならない可能性がある。シノファームとSinovacのワクチンは、既存のコールドチェーンシステムを使用して輸送できる第III相試験中の不活化ワクチンの例であるが、CoronaVac自体は凍結する必要はない。
開発中のmodRNAワクチン技術は、大量生産や分解の制御が難しく、超低温での保管や輸送を必要とする場合がある。例として、モデルナのRNAワクチン候補は、氷点下ぎりぎりの温度でコールドチェーン管理をおこなったとしたら保管期間が制限されてしまう。BioNTech-PfizerのRNA候補は、ワクチンの製造から接種までの輸送保管中、-70℃以下での保管を必要とする。
ワクチンバイアルには数回分のワクチンが入っているが、はじめの投与のために穿刺された後は時間制限があり、それを超えると廃棄されなければならないため、現地での低温保管と接種プロセスの管理に注意を払う必要がある。COVID-19ワクチンは、初期展開の間、多くの場所で供給が不足する可能性が高いため、保健当局、各機関および接種スタッフは、供給量が十分な他の一般のワクチンにおいては供給量の30%程度にものぼる腐敗・廃棄処分を、可能な限り回避する事が求められている。
コールドチェーンはさらに、バイクやドローンなどの地方コミュニティにおけるワクチンの輸送の方法、ブースター投与の必要性、希釈剤の使用、医療従事者、子供、高齢者などの脆弱な人々へのアクセスによっても課題となっている。
国によってはワクチンの長期保管に対応した超低温冷凍庫の数が限られていることや、接種が夏期となるため冷凍庫から接種会場までワクチンを小分けして運べる保冷機材も必要となり、費用の負担が大きい。コールドチェーンの末端では医薬品の専門家以外も多く関わることから、機材の不適切な取り扱いにより低温が維持出来なくなり廃棄に至った事例もある。
航空輸送・陸上輸送
国際航空貨物の調整は、COVID-19ワクチンの、時間と温度に敏感な配布に不可欠な要素であるが、2020年9月の時点では、航空貨物ネットワークは多国籍展開の準備ができていない。「COVID-19ワクチンを安全に届けることは、世界の航空貨物産業にとって今世紀の使命となるだろう。しかし、それは慎重な事前の計画なしには実現しない。そして、そのための時期は今だ。私たちは、各国政府に対し、物流チェーン全体での協力を促進するために主導権を握ることを強く求め、施設、セキュリティの手配、および国境手続きが、前途多難で複雑なタスクに備えられるようにする」と、国際航空運送協会(IATA)の事務局長兼CEOであるアレクサンドル・ドゥ・ジュニアックは2020年9月に発言した。
2020年、旅客航空交通量の深刻な減少のために、航空会社は経費を抑えるため人員の削減(レイオフ)、路線の縮小、航空機の保管・売却などで対応していた。WHO COVAX施設内でのCOVID-19ワクチンの調達と供給の主導機関として、GAVIアライアンスとユニセフは、これまでで最大かつ最速のワクチン展開に向けて準備を進めており、国際的な航空貨物輸送の協力、税関と国境管理、そして複数の国に1回分のワクチンを届けるための8,000機もの貨物機を必要とする可能性がある。
安全保障と汚職
医薬品は世界最大の市場であり、年間約2,000億ドルの価値があるため、COVID-19ワクチンの広範な需要は、サプライチェーン全体で模倣品、盗難、悪徳商法、サイバー攻撃に対して脆弱である。偽造ワクチンと本物のワクチンを識別し追跡するための技術的能力の低さ、アクセスの制約、効果的でない能力など、各国間で調和のとれた規制の枠組みが存在しないことは、ワクチン接種を受ける者の命を脅かす可能性があり、COVID-19のパンデミックを永続させる可能性がある。包装資材に用いる追跡システム技術は、サプライチェーン全体でワクチンバイアルを追跡するため、製造業者によって使用されており、また、ワクチン接種チームのセキュリティを保証するためにデジタルおよび生体認証ツールを使用している。
2020年12月、インターポールは、犯罪組織がワクチンのサプライチェーンに潜入し、物理的手段で製品を盗み、情報窃盗を行い、さらには偽造ワクチンを供与する可能性があると警告した。
国のインフラ整備
WHOは「効果的なワクチン管理」システムを実施しているが、これには、ワクチン配布のための国・準国家の人員や施設を準備するための優先順位を構築することが含まれており、これには以下のようなものがある:
- 時間や温度に敏感なワクチンを扱うスタッフの育成
- ワクチンの保管と輸送を最適化するための堅牢なモニタリング機能
- 温度管理された設備・機器
- トレーサビリティ
- セキュリティ
個々の国内での効率的な取扱い、及び通関のための国境プロセスには、以下のものが含まれる:
- 離陸と着陸の許可を容易にする
- 航空乗務員の検疫要件の免除
- 効率的な国内展開のための柔軟な運用の促進
- ワクチン温度要件を維持するための着陸優先権の付与
ワクチン有効期限
事例としてファイザー製(トジナメラン、ファイザー - バイオンテック、BNT162b2、コミナティ筋注)は超低温冷凍庫(マイナス90℃ - 60℃)での保管でも製造日から有効期限6か月(ただし、2021年9月10日発行の同ワクチンの添付文書第6版においては、マイナス90℃ - 60℃保管の場合の有効期限が6か月から9か月に延長されている)、一般低温冷凍庫で保管可能なモデルナ製(mRNA-1273、スパイクバックス筋注)でも現場到着後2 - 3か月程度が限度であり、需要と供給を見据えた在庫・流通管理が重要となる。
2021年10月頃までに、一部の先進国では住民の2回目までの接種がある程度の割合まで一巡し、接種率の伸びが頭打ちになると共に、予め多めに確保していたワクチンに余剰が出る見通しがでてきた。欧米諸国では2021年末までに約2億回分が、日本でも2022年3月末までに約1億回分が有効期限切れに到達する見通しである。有効期限の迫った余剰ワクチンを不足する国へと国際的に融通しあう枠組みの構築が叫ばれている。
ファイザー製では有効期限が9か月に延長されているが製品ごとに有効期限日が打刻されており既存品の期限延長は原則として行わない。ただし、島根県松江市では、専門医による同市の予防接種委員会の見解として有効性や安全性に問題なしとし、延長された期限内であれば問題ないとして今後も接種する方針である。
ワクチンの確保・接種状況
世界の概況
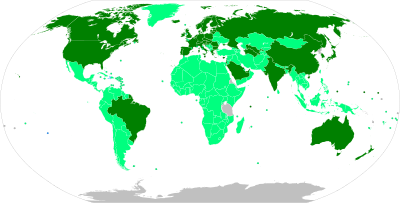
2021年4月10日時点での世界でのCOVID-19ワクチンの接種状況は以下の通り。
100人あたりの接種回数 / 累計接種回数
- イスラエル 112.5 / 10,189,198
- セーシェル 104.6 / 102,080
- UAE 89.1 / 8,707,073
- パラオ 74.6 / 13,435
- ブータン 61.7 / 470,976
- チリ 60.1 / 11,396,072
- 英国 56.1 / 37,736,162
- バーレーン 53.6 / 879,825
2021年3月下旬時点で、日本の100人あたりのワクチン接種回数は0.4回であり、OECDの37か国中で最下位であった。
2021年9月5日時点での世界でのCOVID-19ワクチンの接種状況は以下の通り。
100人あたりの接種回数 / 累計接種回数
- イスラエル 155.2 / 14,050,538
- セーシェル 147.0 / 143,490
- UAE 187.7 / 18,339,225
- パラオ 162.0 / 29,165
- ブータン 137.0 / 1,045,074
- チリ 154.8 / 29,331,816
- 英国 137.0 / 92,213,900
- バーレーン 152.3 / 2,499,774
2021年9月5日時点で、日本の100人あたりのワクチン接種回数は107.5回であり、3月から半年足らずで累計1.3億回を超えて急速に進んだ。
日本
日本国内のワクチン接種率に関しては、2021年10月4日時点で、ワクチンの2回目接種済人数が全人口の60.9%、1回目完了では71.3%であった。NHK報道によるイギリスの統計任意団体「Our World in Data」の調べによれば、各国の保健当局が予定した接種回数(通常2回、国により3回)までの接種率(接種済人数の人口比統計)では、日本は同年10月17時点統計で66.47%と、イギリスの65.7%、ドイツの65.15%、米国の56.17%を抜いており世界的にも遜色のないレベルとなっている。
イスラエル
2021年3月時点でも4月時点でも人口当たりのCOVID-19ワクチンの接種率が世界一となっているのはイスラエルである。ユダヤ人ディアスポラとのコネクションを通じてファイザー社の経営幹部から大量のワクチンの優先的な提供を受ける約束をリークすることにより、政治的不安定に直面するネタニヤフ首相の挽回戦略だとメディアが分析した。2021年8月に3回目接種を、2022年1月3日に4回目接種を開始した。
イスラエルのコロナワクチン対策専門家チーム代表で、イスラエル国内最大の保健機構「クラリット」のチーフ・イノベーション・オフィサーでもあるラン・バリチェルが2021年3月24日に、日本記者クラブ主催のリモート講演会で語ったところによると、「昨年(2020年)の12月19日から高齢者優先で始まったワクチン接種は、16歳以上の全住民に対象が拡大され、イスラエル国民約920万人の60%が既に既に接種済みで、50%が2回接種済み。特に50歳以上は80%が2回目の接種を受けており、高齢者はワクチンで守られている」とのことであり、イスラエルが世界で最も早くワクチン調達できた理由は「昨年の12月より前にワクチンメーカーと事前購入契約を結んでいた。さらに感染が増えた場合にはファイザーや、ほかのメーカーと優先的に提供してもらう契約をしていた。」と説明。そして「その代わり、感染に関するデータは世界で共有するという条件が付いていた。つまりイスラエルがワクチン接種の『テストベッド』になることで大事なワクチンをより早く調達できた」と説明した。
イスラエルでのワクチン接種のしかたについては、「イスラエルではワクチン接種するためにワクチンクリニックを各地にオープンした」と言い、数百というクリニックを1週間でイスラエル全土に展開した、という。大きな病院や広場にテントを張るなどしてクリニックを設営し、接種を受けた人の管理は、20年前にデジタル化した電子カルテを使って行い、誰が接種を受けたか、2回目の接種の日時の案内も1回目を受けた時点で決まるようにした、と言い、イスラエルではデジタル化が進展していることが効率的なワクチン接種に大いに役立ったと明かした。また「透明性の確保が重要だった。われわれが知っていることと、分からないことをクリアなメッセージとして隠さず国民に伝えた。」と語った。
接種を促進する手法については「接種を受けた人には『グリーンバッジ』を付けてもらっている。」と説明。「スマホで接種を受けたことを証明するマークを受信しておけば、レストランの店内で食事ができ、コンサートや文化イベント等にも参加可。それに対して、接種を受けていない人はレストランの店外でしか食事ができないとするなど、接種を受けた人と受けてない人に違うルールを適用したことで、経済活動を安心して再開することができ、接種を増やすインセンティブにもなった」と説明。
アメリカ合衆国
アメリカ合衆国は2021年7月時点で、総人口に対するワクチン接種率が49%で頭打ち傾向にある。アメリカ合衆国大統領ジョー・バイデンは同年7月29日の演説で、アメリカ合衆国連邦政府の財政負担により、各地方当局がワクチン接種者に100ドルを給付して接種を促すよう呼びかけたほか、連邦政府の職員と取引企業従業員に対する接種状況開示の義務化を表明した。
ワクチン接種者・非接種者の処遇
COVID-19ワクチンを接種済みであるか未接種であるかの明示や、職種によっては接種を義務化する国もあり、医学的な理由や自由意思で接種を受けない人との取り扱いの差をどうするかという課題も浮上している。米国政府は2022年1月4日から、従業員数が100人以上の企業など接種を義務付けると2021年11月4日に発表した。これに先立って、同国ニューヨーク市が接種しない職員の無給休暇扱い(医学・宗教上の理由を除く)を表明したところ、抗議デモが起きた。
日本では厚生労働省が雇用や求人における指針をホームページで公表しており、接種拒否だけを理由とした解雇や雇い止めは許されないといった基準を示している。
ワクチン・パスポート
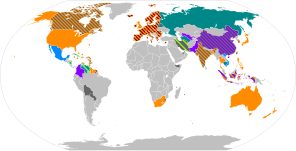
COVID-19ワクチンの接種証明書(ワクチン・パスポート)を発行する国もあり、2021年2月に世界で最も接種が進んでいるイスラエルが、翌3月には中国が開始 し、各国もこれに続くとされている。同年4月1日時点でヨーロッパの一部諸国(アイスランド、エストニア、キプロス、ジョージア、ポーランド、ルーマニア)、中南米でグアテマラやベリーズ、エクアドル、インド洋の島国セイシェルといった国々が、ワクチン・パスポート保持者の旅行入国解禁を開始している。但し、国によっては接種したワクチンの製薬会社によって有効・無効の違いがある。
また、ワクチン・パスポートを得るために渡航するワクチンツーリズムも始まっている。
日本では、2021年7月26日から、海外渡航者を対象に、ワクチン接種の事実を公的に証明する証明書の交付申請の受け付けを各市区町村で開始する。ただし、日本への帰国時の検疫措置の緩和はない。
子供への接種
何歳から接種対象とするかの判断は国によって分かれるが、デメリット(副反応)よりもワクチンを接種するメリット(重症化予防、家族への感染拡大予防など)が大きく上回るという判断は各国で共通している。
アメリカやカナダ、フランス、イスラエル、日本などでは全ての5 - 11歳の小児にワクチンの接種を推奨している。アメリカでは2022年5月に5 - 11歳への3回目のブースター接種が推奨され、6月には生後6カ月からの接種が推奨された。カナダや香港でも2022年8月から生後6カ月からの接種が始まった。
2022年8月11日時点でオーストラリアの5 - 15歳の2回接種率は約55%、アメリカの5 - 11歳の2回接種率は30.1%、カナダの5 - 11歳の2回接種率は42.44%、日本の5 - 11歳の2回接種率は18.5%となっている。
EU諸国における2022年8月11日時点の5 - 9歳の2回接種率は、スペイン31.3%、ポルトガル31.0%、デンマーク28.8%、アイスランド28.1%、オーストリア22.0%、アイルランド20.6%である。ドイツは、健康な5 - 11歳の子どものほとんどが1度はCOVID-19に感染したことがあるため、1回の接種で十分に免疫を獲得できるとし、すべての子どもに1回の接種を推奨している。また、基礎疾患を持つ子どもは3回目のブースター接種を、リスクのある人と同居・接触する子どもには2回の接種を推奨する。ドイツの5 - 11歳の接種率は2022年5月24日時点で22%である。
賠償責任
いくつかの政府は、以前のパンデミックのように、COVID-19ワクチンおよび治療薬に関する過失請求からファイザーやモデルナなどの製薬会社を保護することに合意し、政府もその責任を負った。
2020年2月4日、アメリカではアレックス・アザー米保健福祉長官がCOVID-19に対する医療対策として「公共の準備と緊急事態への備えに関する法律」に基づく通知を公表した。宣言は「COVID-19、またはSARS-CoV-2やその変異ウイルスの感染の治療、診断、治癒、予防、緩和に用いられるあらゆるワクチン」を対象に、「故意の不法行為がなければ、ワクチン製造における製造者の過失、または誤った用量を処方した医療従事者の過失を主張する賠償請求は、除外される」としている。この宣言は米国では2024年10月1日まで有効である。
2020年12月、英国政府はファイザーにCOVID-19ワクチンに関する法的補償を与えた。欧州連合では、COVID-19ワクチンは、民事および行政責任の請求から製造者を免除しない条件付き販売認可の下で認可されている。ワクチン製薬会社との購買契約は秘密のままであるが、認可の時点で知られていなかった副作用に対しても、責任免除の内容は含まれていない。
日本においては、他のワクチンと同様に副反応による健康被害が起きた場合、予防接種法に基づく国の救済制度の対象とされる。
誤った情報
SNSでは、COVID-19ワクチンが利用できなかった時期に「既に利用可能である」という陰謀論も見られた。様々なSNSの投稿で引用された特許には、SARSコロナウイルスなどの他の株の遺伝子配列やワクチンに関する既存の特許が参照されているが、COVID-19については参照されていない。
2020年5月21日、「nCoV19 spike protein vaccine」と称するワクチンを販売していた、米国シアトルに本拠を置くNorth Coast Biologics社に対し、アメリカ食品医薬品局(FDA)は中止通知を送ったことを公表した。
オーストラリア戦略政策研究所(ASPI)は、西側で開発されたワクチンに関わるフェイクニュースあるいはプロパガンダを中国・ロシアが流布していると主張している。国際的なNGO「デジタルヘイト対抗センター」は、英語圏で反ワクチン発信をするインフルエンサーが広告などで巨額の利益を得ている可能性を指摘している。
他のワクチンに関するデマとしては、次のようなものが挙げられる。
- 不妊になる。
- コロナワクチンにはRFIDタグやマイクロチップが混入されており、政府がタグやチップを埋め込んで人間を管理する。
- コロナワクチンを接種するとBluetoothを通じて周辺機器にインターネット接続される。
- 5G通信に接続される。
- 身体が磁石になる。
- ヒト免疫不全ウイルス(HIV)に感染する
- 自閉症を引き起こす。
- mRNAワクチンを接種したらヒトDNAが改変される。
- 政府が遺伝子操作しようとしている。
2021年7月19日の読売新聞オンラインの報道 では、「英NPO『反デジタルヘイトセンター(CCDH)』の調査によると、SNS上のワクチンに関するデマの65%は、12の個人・団体が発信源」とし、発信源には元アメリカ合衆国司法長官ロバート・F・ケネディの息子のロバート・F・ケネディ・ジュニアも含まれるとしている。対策として、FacebookやTwitterで、保健機関が否定した情報の削除、リツイートや「いいね」機能の停止などの措置が行われている。
日本での誤情報
日本では医療従事者へのワクチン先行接種が始まったのとほぼ同時期の2021年2月頃から「ワクチン接種で不妊になる」旨のTwitter投稿が拡散し始めた。その半数は7つのアカウントが起点になっており(東京大学教授鳥海不二夫の分析による)、他の主張も反グローバリズムや陰謀論の傾向がみられた。
武田邦彦はYouTubeの番組で、イギリスのワクチン接種の結果から「日本の高校生320万人全員にワクチンをうったら、確率的には50人が死亡するか、それに相当する副作用に見舞われる」と発言した。しかし、イギリスにおいて、ファイザー社・アストラゼネカ社のワクチンを接種したこととの因果関係が認められる死亡例や、それに相当する副反応は報告されておらず、武田の発言は誤りである。
また、日本国内においてはしばしば厚生労働省が発表する接種後の死者数を引用して「COVID-19ワクチン接種後に多くの人が死亡しており危険」などという風説が流布されることがあるが、厚生労働省が公開している事例はあくまで副反応疑い報告制度に基づき報告のあったものの件数であり、ワクチン接種直後に死亡した者の総数とも、あるいは接種と死亡の因果関係が認定された者の総数とも一致しない。
似たような風説で、「厚生労働省が発表するCOVID-19ワクチン接種後の死亡者の殆どは、接種と死亡の因果関係が不明と結論づけられており、このようなワクチンは信用できない」というものもあるが、これは日本国内における行政解剖の件数が極めて少ないという、COVID-19ワクチンに限らない問題が原因でもあり、インフルエンザワクチンにおいても同様の事象がかねてより発生している。ただし、上記の通り解剖による直接的な死因究明があまり行われていないことは事実ではあるものの、プラセボ対照試験においてワクチン群ととプラセボ群の間に重篤な有害事象の発現頻度の差がないことは既に実証されている。
なお、副反応疑い報告制度に基づいて報告のあった案件は、厚生労働省の審議会に報告され、専門家による審査が行われるが、2021年10月時点で、日本国内においてCOVID-19ワクチンの接種と死亡に因果関係が認定されたケースは皆無である。 このため厚生労働省では「安全性において重大な懸念は認められない」との評価を下しており、一般市民向けのQ&Aサイトにおいては「新型コロナワクチンの接種が原因で多くの方が亡くなったということはありません。」と説明している。
大阪の通天閣のネオンサインを「治験中 射ったらあかん」「射っちゃダメだよ」〔ママ〕と改竄した2枚の画像が、2021年11月にTwitter上で拡散された。COVID-19ワクチンを接種しないよう呼びかけるために改竄したとみられ、運営会社は公式Twitter上で「悪質なデマ」として注意喚起している。
ワクチンに関する真偽不明あるいは明らかな誤情報の拡散は反ワクチン思想や陰謀論を主張する一般アカウントにとどまらず、同様の思想を持つ医療関係者、研究者、論客のほか政治家といった公人による発信もしばしばみられる。
その中でも、元内閣総理大臣の鳩山由紀夫は2022年7月13日に自身のTwitterで、(医師から聞いた話として)「WHOがワクチンを打った人の方が打たない人より3倍入院する確率が高いことを認めたとのこと。ファイザーは大量のデータを消したとの内部告発も発表された。今までワクチン利権は聞いていたが、陰謀論と切り捨てられるようなものではないことが明らかになった」とツイートし、投稿がSNS上で拡散された。これに対し、元新型コロナワクチン接種推進担当大臣の河野太郎は「元首相がワクチンデマを流していた。いったい何が起きたんだろう」と鳩山を批判するツイートを行い、BuzzFeed Japanによるファクトチェックにおいても、鳩山のツイートは専門家によって事実が否定されており、「国民の命・健康と生活に関わる情報については特に、情報の真偽と発信が及ぼす影響について、発信者も十分に注意することが大切であり、元首相のように影響の大きな人物は自らの発する情報の正確性には十分注意してほしいと思います」と釘を刺している。 しかし、その後も鳩山は9月14日にTwitter投稿でも「白澤卓二先生(国際予防医学協会理事長)にあらためて訊きました。WHOがワクチンで重症になる確率はコロナで入院する確率の3倍とWHOが認めたのは事実ですかと。河野太郎大臣はデマと否定されましたがと。白澤先生は事実ですと答えられました。私はアンチエイジングの権威の白澤先生の言葉を信じます」と再びワクチン接種に対する根拠の乏しい持論を展開し、各メディアのファクトチェックでも誤りとされるなど、総理経験者でもある鳩山の科学的根拠に基づかない軽率なツイートに対して、専門家などから厳しい批判が続いている。
脚注
注釈
関連項目
外部リンク
全般
- 新型コロナワクチンについて - 厚生労働省
- コロナワクチンナビ - 厚生労働省
- 厚生科学審議会 (予防接種・ワクチン分科会) - 厚生労働省
- 新型コロナワクチンの接種後の健康状況調査 - 厚生労働省
- 新型コロナワクチンについて - 総理大臣官邸
- 新型コロナワクチンの接種状況 - デジタル庁
- COVID-19ワクチンに関する提言 - 日本感染症学会
- 新型コロナワクチンに関する情報 - 国立感染症研究所
- NHK特設サイト「新型コロナウイルス:ワクチンQ&A」 - NHK
- 新型コロナウイルス ワクチン接種始まる - NHK放送史
- 新型コロナウイルス感染症(COVID-19)の研究開発課題について - 日本医療研究開発機構 (AMED)
- 製薬協加盟各社による、治療薬・ワクチンの研究開発の取り組みについて - 日本製薬工業協会
- Coronavirus (COVID-19) Vaccinations(英語) - Oxford Martin School
- COVID-19 vaccines(英語) - World Health Organization (WHO)
- COVAX(英語) - World Health Organization (WHO)
- COVAX Facility(英語) - Gavi
- Vaccines for COVID-19(英語) - アメリカ疾病予防管理センター (CDC)
小児
- 5~17 歳の小児への新型コロナワクチン接種に対する考え方 - 日本小児科学会 2022/8/10更新
- 「新型コロナワクチン~子どもならびに子どもに接する成人への接種に対する考え方~」に関するQ&A - 日本小児科学会 2022/5/31更新
- 新型コロナワクチンQ&A 小児接種(5~11歳) - 厚生労働省
- 子供と10代の若者がCOVID-19のワクチン接種を受けるべき理由 - アメリカ疾病予防管理センター(CDC) 2022/7/21更新(英語)
- 子どものためのワクチン COVID-19 - カナダ政府 2022/7/14更新(英語)
- 小児に対するCOVID-19ワクチン接種に関する中間声明 - WHO 2022/8/11更新(英語)
|
新型コロナウイルス感染症 (COVID-19)
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| SARSコロナウイルス2 |
|
||||||||||||||||||
| 治療 |
|
||||||||||||||||||
| 感染拡大 | |||||||||||||||||||
| 影響 (コロナ禍) |
|
||||||||||||||||||
| 社会の対応 |
|
||||||||||||||||||
| 組織 |
|
||||||||||||||||||
| その他関連項目 | |||||||||||||||||||


![SARS-CoV-2に採用されているワクチンのプラットフォーム。全ウイルスワクチンには、弱毒化されたウイルスと不活性化されたウイルスの両方が含まれる。タンパク質およびペプチドサブユニットワクチンは通常、免疫原性を高めるためにアジュバントと組み合わされる。SARS-CoV-2ワクチン開発では、三量体のスパイクタンパク質全体、または受容体結合領域(RBD)などの構成要素を使用することに重点が置かれている。複数の非複製ウイルスベクターワクチンが開発されており、特にアデノウイルスに焦点が当てられている。一方、複製ウイルスベクターのコンストラクトはあまり重視されていない。[177]](http://upload.wikimedia.org/wikipedia/commons/thumb/e/ee/Fimmu-11-579250-g004.jpg/234px-Fimmu-11-579250-g004.jpg)